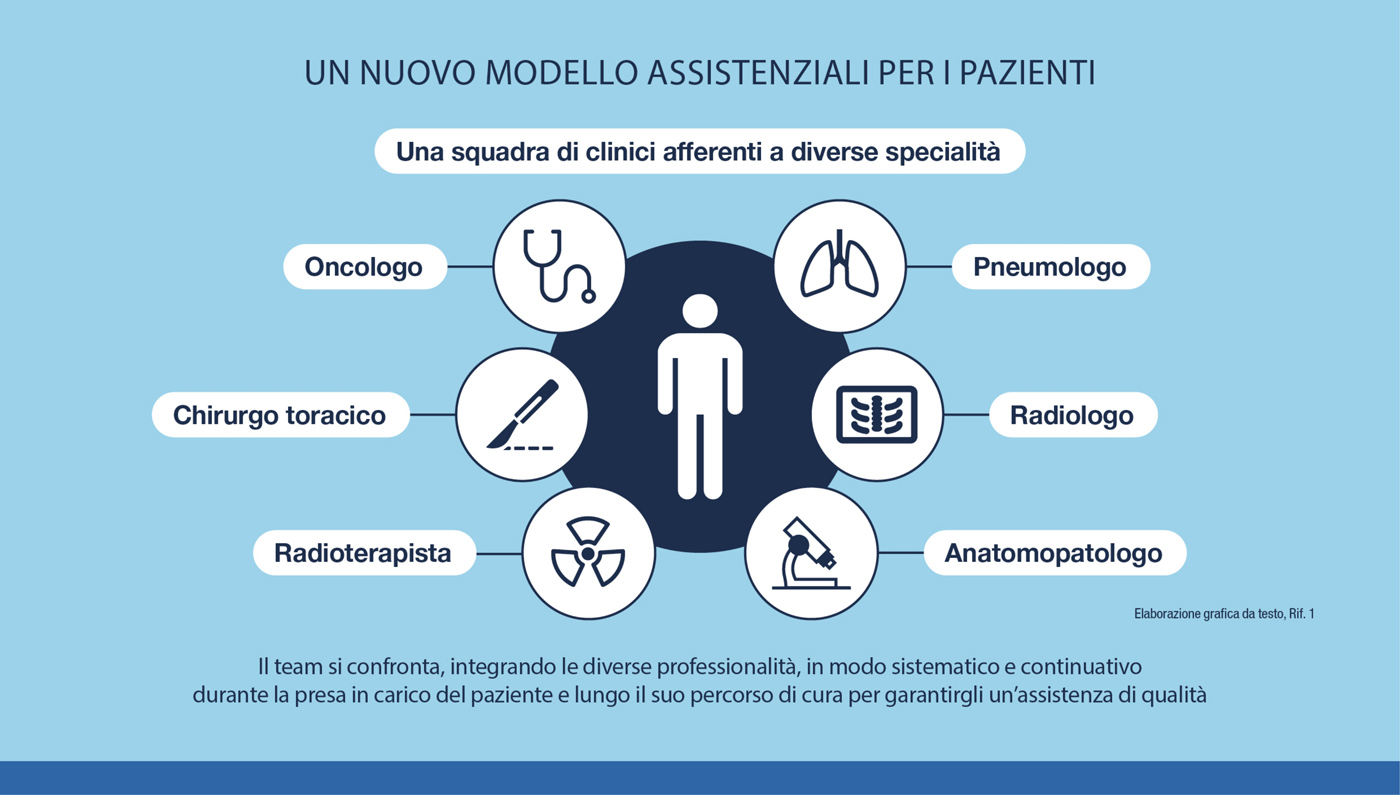
La gestione del carcinoma polmonare richiede la partecipazione di diverse figure specializzate per assicurare una cura ottimale al paziente, per questo è importante la presenza di un team multidisciplinare. 1
Diversi studi hanno analizzato l’impatto positivo del team multidisciplinare su numerosi parametri.
In particolare, uno studio condotto su >4000 pazienti ha dimostrato che:2
- la diagnosi e il trattamento del tumore al polmone gestiti da un team multidisciplinare si traduce in un significativo beneficio in termini di sopravvivenza.
Inoltre, l’applicazione del modello del team multidisciplinare permette il superamento di barriere relative ai trattamenti, promuove la prescrizione di terapie standardizzate attraverso l’aderenza alle linee guida e per queste ragioni fornisce un’assistenza di qualità per i pazienti con carcinoma polmonare3.
BIBLIOGRAFIA
- Prabhakar CN et al, Respirology, 20 (6), 884-8
- Bilifinger TV, et al. Clin Lung Cancer. 2018 Jul;19(4):346-351
- Denton E, et al. J Multidiscip Healthc. 2016;9:137-44
Elaborazione grafica da testo, Rif. 1
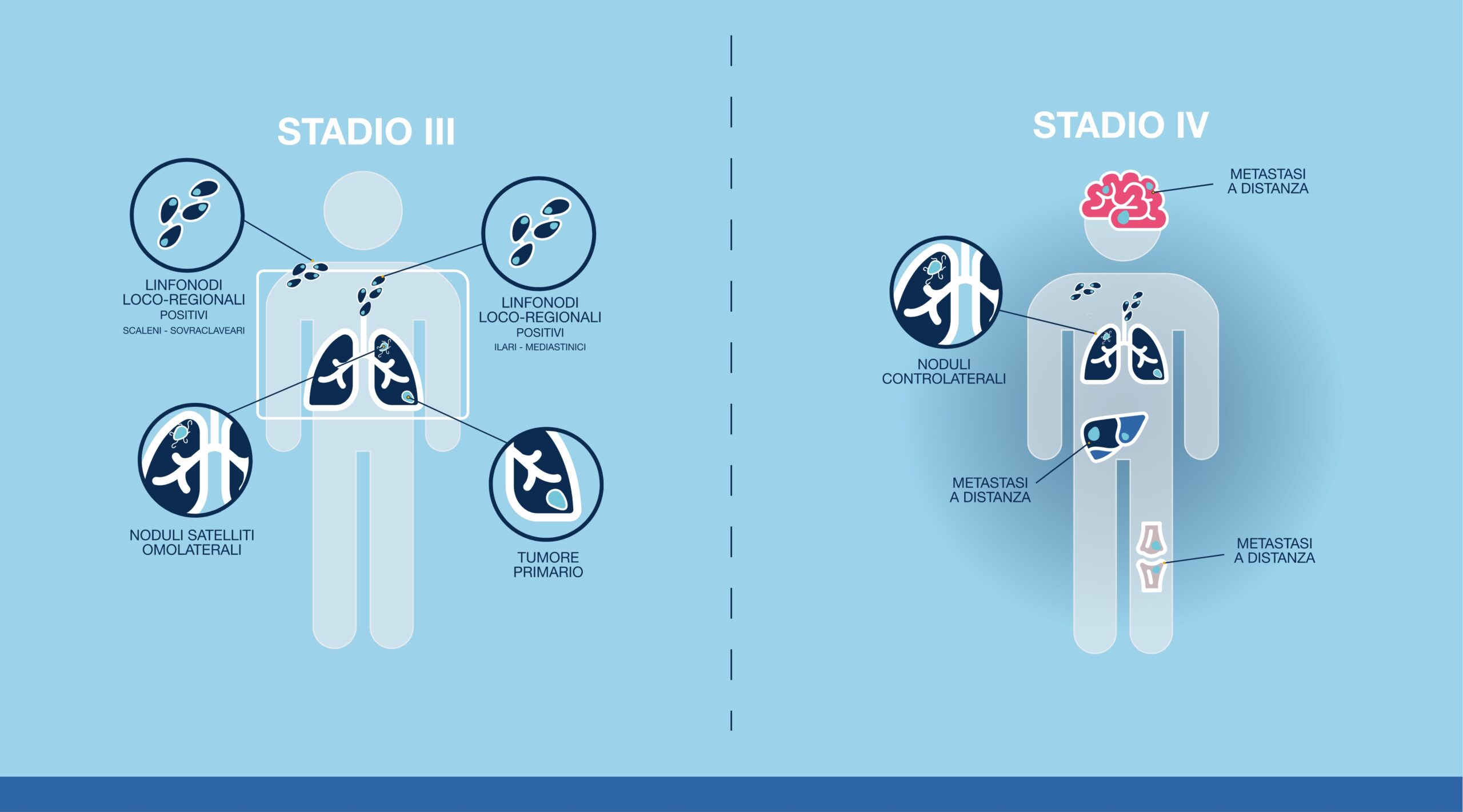
Lo stadio del tumore è definito da diverse caratteristiche fisiologiche: 1

STADIO III
Il tumore si può presentare con diverse combinazioni delle tre caratteristiche citate; la sua dimensione può essere variabile e iniziano a essere coinvolti i linfonodi loco-regionali più o meno lontani. Nello stadio III il tumore è ancora localizzato all’interno del torace.
STADIO IV
Il tumore ha iniziato la sua diffusione, si ritrovano quindi metastasi in altri organi. Nello stadio IV è possibile che siano presenti metastasi in un solo organo (ad esempio il cervello) o in più organi contemporaneamente (ad esempio cervello, ossa, fegato, ecc…)
BIBLIOGRAFIA
- AIOM Linee Guida NEOPLASIE DEL POLMONE. Edizione 2018.
SOMMINISTRAZIONE: 1
Gli immunoterapici vengono tutti somministrati per infusione endovenosa, con uno schema preciso in base al tipo di trattamento.
Per l’infusione è sempre necessario andare in ospedale e la somministrazione del farmaco dura circa un’ora e mezza.
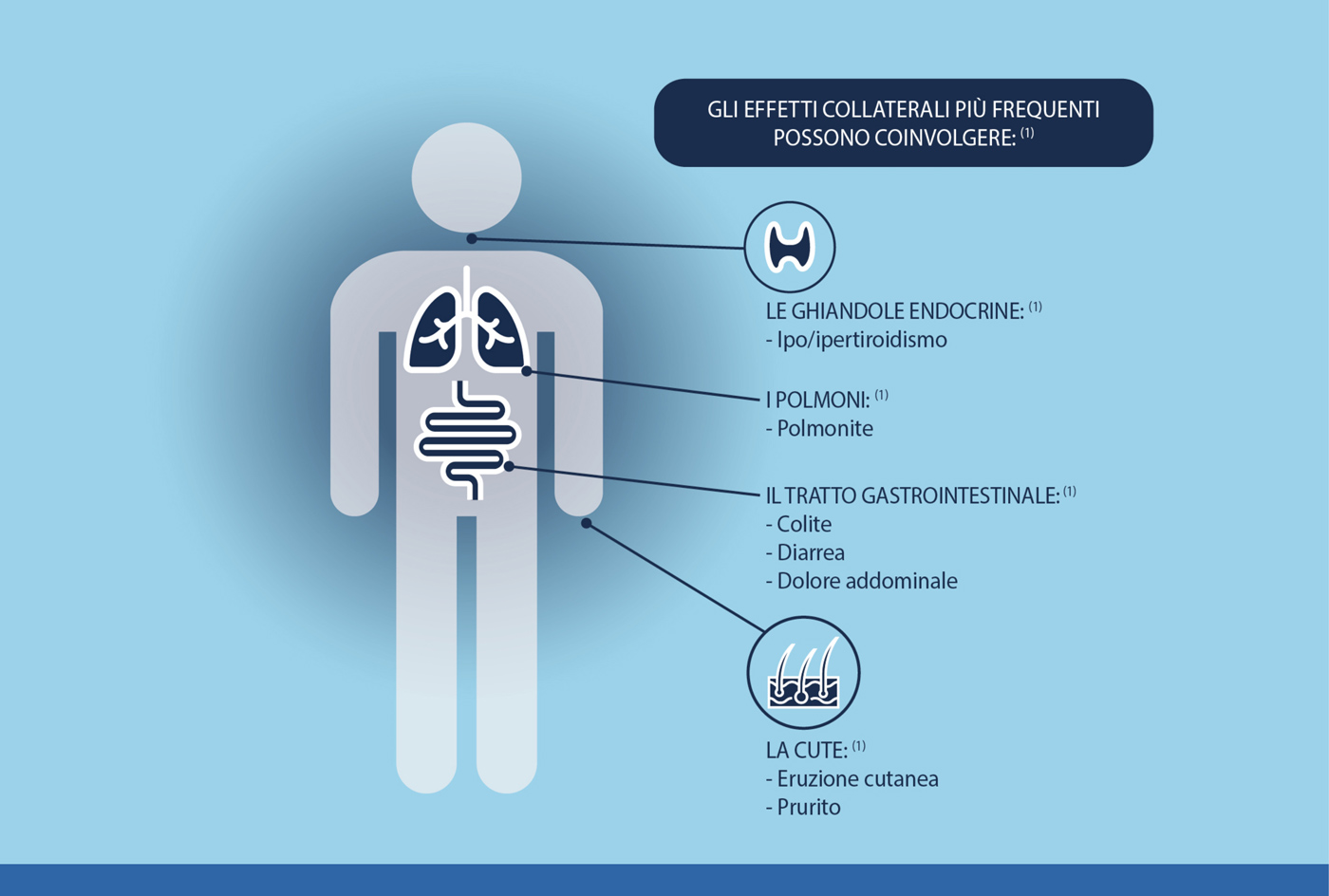
EFFETTI COLLATERALI: 1
Gli effetti collaterali dell’immunoterapia sono differenti rispetto a quelli provocati dalle altre terapie contro il cancro. Non tutti i pazienti sperimentano lo stesso tipo di effetti collaterali e alcune persone potrebbero non averne affatto. In genere, gli effetti collaterali compaiono entro poche settimane o mesi dall’inizio della terapia, ma possono insorgere in qualsiasi momento.
L’importanza della comunicazione 1
- Una corretta informazione è fondamentale per il riconoscimento e la segnalazione precoce dei segni e sintomi degli effetti collaterali.
- La comunicazione diretta e la stretta interazione tra paziente, oncologo e medico di medicina generale, rendono il trattamento più sicuro, gestibile ed efficace.
- Per il paziente, sapere cosa aspettarsi e come prevenire o gestire gli effetti collaterali può essere d’aiuto per mantenere sotto controllo la situazione e per migliorare la qualità della vita.
Consigli per la vita quotidiana 1
- Chiedi al tuo oncologo tutto quello che desideri sapere a proposito della malattia.
- Fai attività fisica, l’esercizio aiuta a contrastare la stanchezza e favorisce l’appetito.
- Segui una dieta sana.
- Tieni un diario quotidiano del trattamento, scrivendo come ti senti e cosa pensi.
- Ascolta sempre il tuo corpo.
BIBLIOGRAFIA
- Di Giacomi AM, Maio M, Monterisi S. Immunoterapia. Cosa tenere sotto controllo. Una guida pratica per il paziente. Effetti Editore, 2019
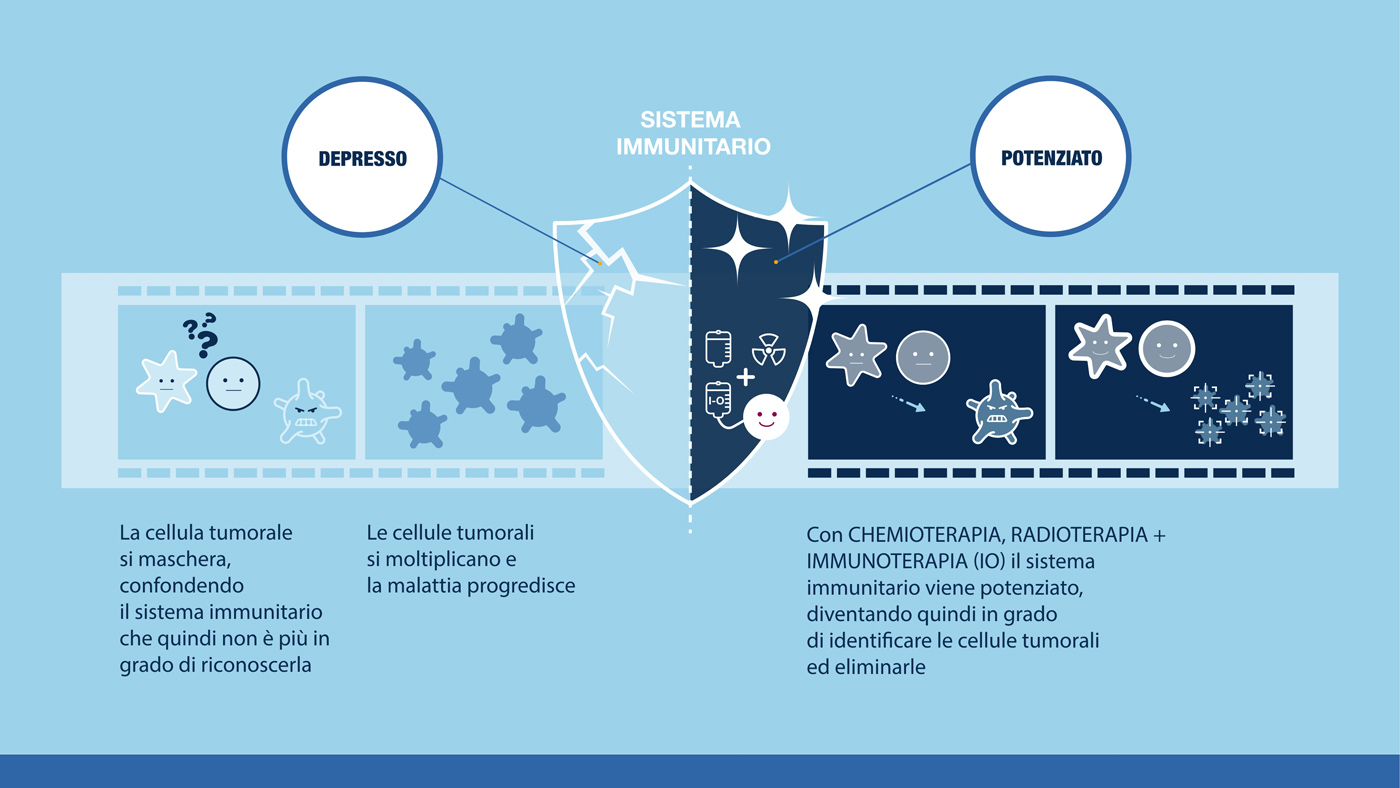
Le cellule tumorali eludono il sistema immunitario mascherandosi e inibendo la risposta difensiva, in questo modo sono in grado di moltiplicarsi in modo incontrollato.1
L’immuno-oncologia non colpisce direttamente le cellule tumorali ma attiva le cellule del sistema immunitario, mettendole nelle condizioni di distruggere il tumore.1 Così facendo impedisce alle cellule malate di sfuggire al controllo del sistema immunitario e mantiene i meccanismi di difesa sempre attivi.1
BIBLIOGRAFIA
- Mauro Boldrini, Sabrina Smererei, Paolo Cabra. Immuno-oncologia. 100 domande 100 risposte. La guida per conoscere la nuova arma contro i tumori e il “pianeta” cancro. Seconda edizione. AIOM.
Ogni tumore è differente e, sulla base dello stadio in cui la malattia si trova, ha bisogno di un diverso tipo di trattamento o di una diversa combinazione di trattamenti.
STADIO I E II
Lo stadio I e II definisce lo stadio iniziale della malattia, non esteso a nessun’altra parte del corpo e di piccole dimensioni, quindi potenzialmente curabile con l’intervento chirurgico. 1
In base alla presenza o meno delle cellule nei linfonodi circostanti il tumore, prelevati durante l’intervento per essere analizzati, si decide se, in seguito all’intervento, è opportuno un trattamento definito «adiuvante» con chemioterapia o radioterapia. 1
STADIO III
Lo stadio III definisce il tumore in stadio avanzato, ma non ancora diffuso in altre parti del corpo. Nello stadio III sono compresi tumori che non presentano cellule tumorali all’interno dei linfonodi, tumori positivi per un numero limitato di linfonodi e tumori con un numero importante di linfonodi coinvolti.1 In base a queste tre caratteristiche, viene identificata la terapia più adeguata: 1
- Se il tumore è considerato operabile si procede con l’intervento chirurgico, preceduto o seguito da chemioterapia e/o da radioterapia.
- Se la chirurgia inizialmente è controindicata perché, ad esempio, la massa è troppo estesa o la posizione è complicata da raggiungere, si interviene con una combinazione di chemio e radioterapia «neo-adiuvante» e, solo in un secondo momento, si considera l’intervento chirurgico.
- Se il tumore è non operabile e quindi l’intervento è da scartare, si procede con il trattamento a base di chemioterapia e radioterapia, anche somministrate contemporaneamente.
Nei pazienti in cui non è possibile procedere con l’intervento chirurgico, nel caso in cui il tumore torni a crescere e ad espandersi dopo trattamenti chemioterapico/radioterapico, si può procedere con l’immunoterapia. 1
STADIO IV
Lo stadio IV definisce una malattia metastatica, cioè diffusa ad altre parti del corpo oltre al polmone.1 In questo caso l’intervento chirurgico non può essere considerato e l’opzione di trattamento preferenziale è la terapia farmacologica che varia in base alle caratteristiche molecolari specifiche del tumore:1
- In assenza di mutazioni genetiche o con bassi livelli di PD-L1 = chemioterapia
- In presenza di mutazioni EGFR, BRAF, ALK o ROS1 = terapie a bersaglio molecolare
- In presenza di elevati livelli di proteina PD-L1 = immunoterapia.
BIBLIOGRAFIA
- Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
La sorveglianza è il processo attraverso il quale il sistema immunitario riconosce i tumori e dà inizio a una risposta anti-tumorale. 1

Sulla superficie delle cellule tumorali sono presenti alcune strutture differenti rispetto a quelle presenti sulle cellule sane: sono i cosiddetti antigeni tumorali, che permettono al sistema immunitario di riconoscere la cellula malata come estranea. 1
- Specifiche cellule del sistema immunitario definite cellule che presentano l’antigene (APC) sono deputate al riconoscimento di questi antigeni estranei. Nel momento in cui le APC individuano una cellula tumorale possono attivare a loro volta i linfociti, i quali sono in grado di attaccare il tumore. 1
- In alcuni casi però le cellule tumorali evadono il controllo del sistema immunitario, generando un ambiente che non promuove la risposta anti-tumorale, definito immunosoppressivo. 2
- Ciò provoca la replicazione delle cellule tumorali in modo incontrollato, determinando così lo sviluppo e la crescita del tumore. 1
Bibliografia
- Boldrini M, Smerrieri S, Cabra P. Immuno-oncologia. 100 domande 100 risposte. La guida per conoscere la nuova arma contro i tumori e il “pianeta” cancro. Seconda edizione. AIOM
- Beatty GL, et al. Immune escape mechanisms as a guide for cancer immunotherapy. Clin Cancer Res. 2015;21(4):687-92
A oggi sono state identificate oltre 12 mutazioni genetiche correlate al NSCLC, alcune delle quali sono più comuni di altre. 1
Tali mutazioni possono insorgere in tutte le diverse forme di NSCLC, ma è stato osservato che sono più frequenti in alcuni specifici gruppi di pazienti. 1
Conoscere la presenza di queste mutazioni è fondamentale per poter scegliere il trattamento più adeguato ed efficace. 1
INCIDENZA DI MUTAZIONI SPECIFICHE NELL’NSCLC 1
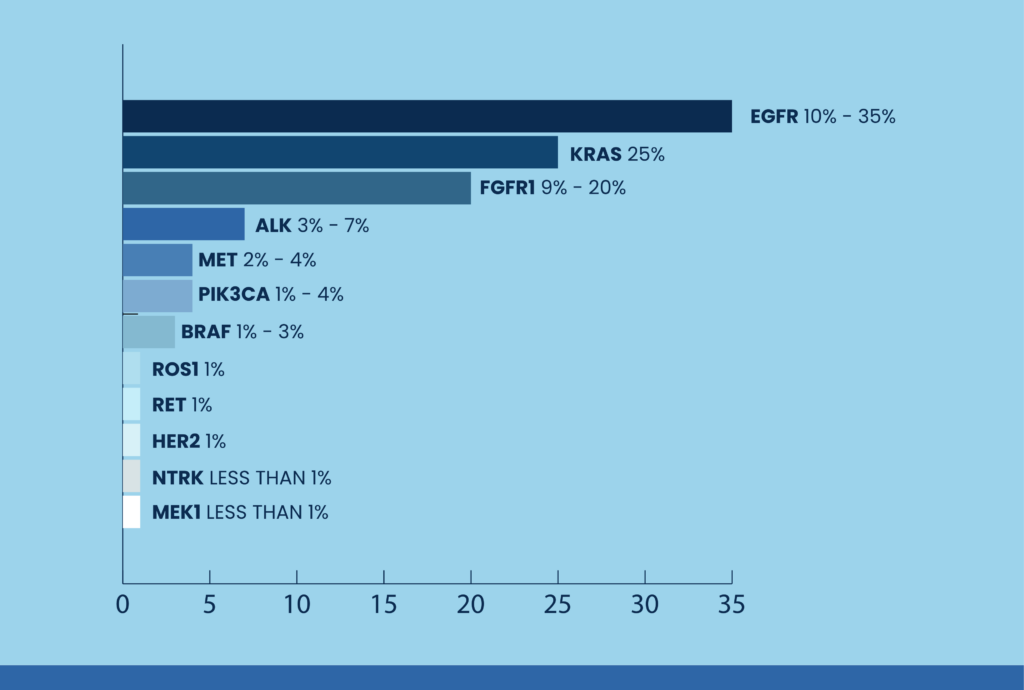
EGFR
Il gene controlla una proteina chiamata recettore per il fattore di crescita epidermico (EGFR) coinvolta nella regolazione della crescita e proliferazione della cellula. È più comune nei pazienti donne, non fumatori, con adenocarcinoma. 1
ALK
È il gene che codifica per la chinasi del linfoma anaplastico; quando è presente tale mutazione due geni si fondono insieme per crearne uno nuovo. Tale mutazione è presente in persone che non hanno mai fumato o hanno ceduto raramente al fumo. È una mutazione molto comune in persone cinquantenni e negli uomini. 1
HER2
Quando questo gene è mutato le cellule tumorali sono spinte a crescere. Questa mutazione si riscontra soprattutto nelle donne e in persone che non hanno mai fumato o hanno fumato raramente. 1
ROS1
Questa mutazione è simile a quella ALK per quanto riguarda le popolazioni colpite: cinquantenni e non fumatori. 1
KRAS
Questo gene permette che venga prodotta una proteina chiamata K-Ras che aiuta le cellule a crescere e a dividersi. 1
NTRK
In coloro che hanno questa mutazione il gene NTRK si fonde con altri geni e non ci sono caratteristiche specifiche negli individui in cui viene trovata: sia fumatori che non e di ogni fascia d’età. 1
RET
Letteralmente è il «gene riarrangiato durante la trasfezione» ed è particolarmente comune nei soggetti non fumatori. 1
PD-L1
Il ligando di morte programmata 1, o PD-L1, è una proteina coinvolta nei meccanismi che il tumore mette in atto per sfuggire alle difese immunitarie del corpo. 2 Per decidere come trattare al meglio un tumore e a quali terapie è possibile sottoporre il paziente è importante valutare in che misura questa proteina è presente nel tumore. 3
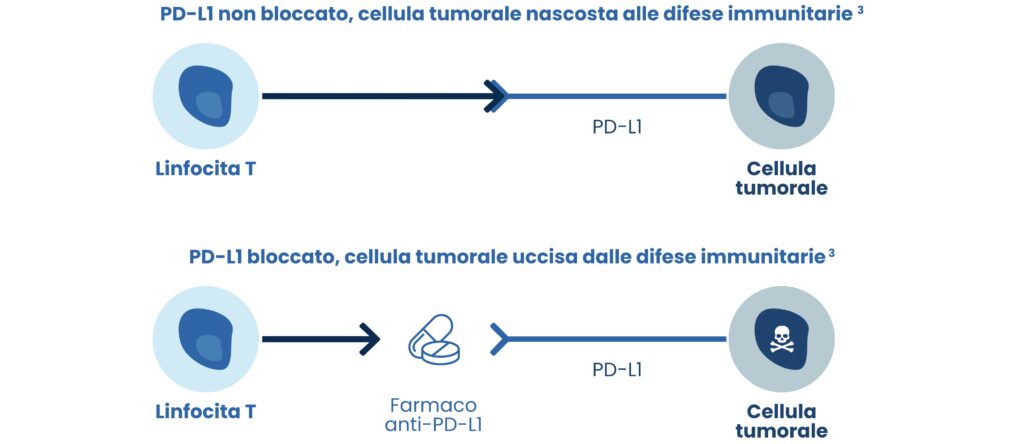
IL RUOLO DI PD-L1
Sulla superficie dei linfociti T, un particolare tipo di globuli bianchi è presente un recettore che, tramite il legame alla proteina PD-L1, riconosce se una cellula appartiene o meno al nostro organismo. 3 Il tumore, grazie alla presenza sulla superficie delle sue cellule di PD-L1, è in grado di legarsi ai linfociti e “mascherandosi” da una cellula dell’organismo, nascondendosi di fatto alle difese immunitarie. I linfociti perciò sono indotti a non riconoscere la cellula come tumorale e non danno avvio al processo di eliminazione delle cellule tumorali. 3 Per far sì che il sistema immunitario torni a riconoscere le cellule tumorali come non appartenenti al corpo si sono sviluppati dei nuovi farmaci detti anti-PD-L1. 3 Tali farmaci si legano a PD-L1 sulle cellule tumorali impedendogli di legarsi quindi ai linfociti che in questo modo possono riconoscere la cellula tumorale come estranea al corpo e attivare la risposta immunitaria. 3
I TEST PER LE MUTAZIONI GENETICHE
Per effettuare i test utili a identificare la presenza di eventuali mutazioni è necessario raccogliere un campione del tumore. Questo avviene con una delle seguenti modalità: 1
- Tramite broncoscopia, ossia prelevando un campione di tumore dal polmone, tramite un piccolo tubicino che si fa passare dalla bocca o dal naso (nessuna paura, si è anestetizzati per la procedura).
- Usando un sottilissimo ago che il medico inserisce direttamente dal petto (si può prelevare anche del liquido dai polmoni). Questa procedura è chiamata agobiopsia transtoracica.
- Una variante di quest’ultima procedura è la VATS, cioè la toracoscopia chirurgica video-assistita. Il medico, invece di inserire un ago nel petto, fa un piccolo taglietto e inserisce un tubicino con cui preleva il tessuto.
- A differenza della VATS, se il taglio viene effettuato in un punto specifico sopra lo sterno, parliamo di mediastinoscopia ma la procedura è simile.

Una volta ottenuto il campione di tessuto tumorale, l’analisi delle mutazioni può essere condotta con le seguenti modalità:
- Immunoistochimica: consente di evidenziare l’espressione di determinate proteine, definite marker tumorali. Serve il tessuto tumorale per fare questo tipo di test. 1
- FISH: è un acronimo che indica un test di fluorescenza che ricerca specifiche variazioni nei geni. Per questo tipo di test può essere usato sia il sangue sia il tessuto proveniente dal tumore. 1
- Test allele-specifico: è un test che permette di analizzare il DNA per una singola, specifica mutazione. 1
- NGS: si tratta di un acronimo che indica ”sequenziamento genetico di nuova generazione” e permette di individuare mutazioni diverse, effettuando però il test una sola volta. È più veloce di altri test e si può effettuare sia su sangue sia su tessuto tumorale. 1
Bibliografia
- Gene mutations in Non-Small-Cell Lung Cancer. Disponibile al sito: https://www.webmd.com/lung-cancer/story/nsclc-gene-mutations
- Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
- Caldwell C. et al. Sci Rep. 2017;7:13682
- Cancer Research UK. FISH testing. Disponibile al sito: https://www.cancerresearchuk.org/about-cancer/cancer-in-general/tests/fish
DNA
Lo studio delle caratteristiche molecolari dei tumori al polmone ha evidenziato un ruolo specifico per alcuni geni, tra cui un gene denominato EGFR. 1
I geni rappresentano importanti bersagli per alcuni farmaci.
La determinazione di mutazioni di EGFR si rende necessaria per la scelta della migliore strategia terapeutica. 1
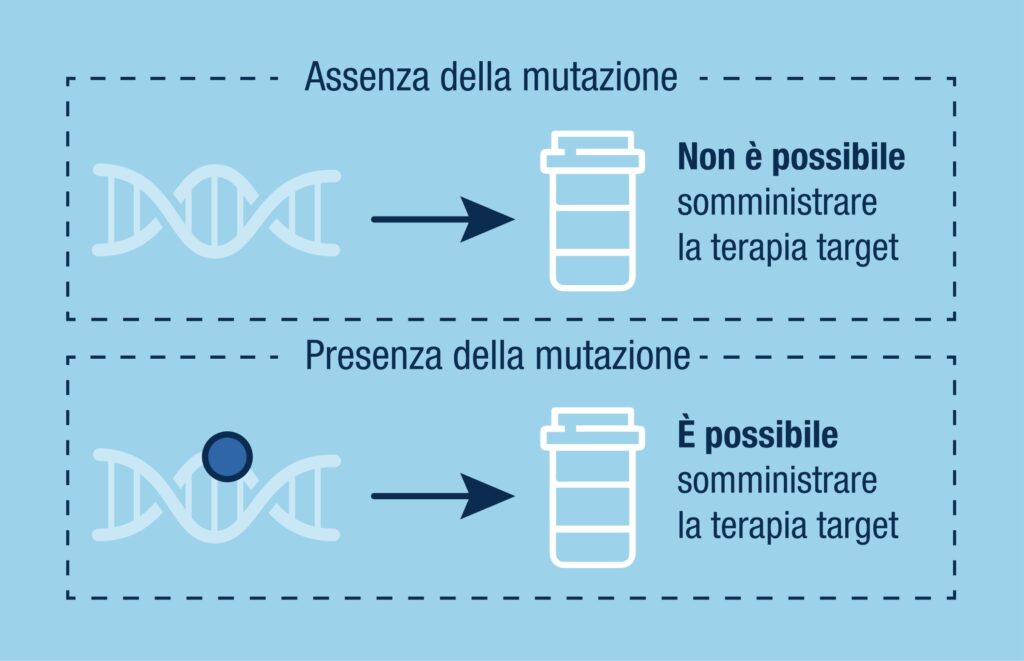
PROTEINE
Nel tumore al polmone è importante inoltre valutare un altro marcatore noto come PD-L1.1
PD-L1 è una proteina presente sulla membrana delle cellule tumorali.2
Valutare la quantità della proteina PD-L1 permette di prevedere l’efficacia dell’immunoterapia.2
COS’È UN MARCATORE BIOLOGICO?
Un marcatore biologico o biomarcatore è un indicatore che può essere misurato in modo affidabile e che ci può dare informazioni riguardo lo stato di malattia dell’individuo.
I biomarcatori possono essere:
- Variazioni nella sequenza del DNA
- Sostanze biologiche di origine proteica, rilevabili nel sangue o in campioni di tessuto
L’identikit molecolare del tumore al polmone si effettua valutando alcuni biomarcatori, utili per predire se un paziente risponderà o meno a una specifica terapia. 1
- La valutazione delle mutazioni del gene EGFR è utile per valutare la prescrizione di una terapia specifica, definita a bersaglio molecolare. 1
- La valutazione del livello della proteina PD-L1 è uno dei parametri che viene preso in considerazione per la scelta del trattamento nei pazienti con NSCLC; in particolare per poter somministrare l’immunoterapia. 1
Bibliografia
- Linee Guida AIOM. Tumore al polmone. 2019
- IASCL atlas testing od PD-L1 immunoistochemistry testing in lung cancer. Edited by MS Tsao, et al. 2017
Il NSCLC origina dalle cellule epiteliali dei polmoni, dai bronchi centrali agli alveoli terminali. 1
Le tre principali forme di NSCLC sono l’adenocarcinoma, il carcinoma a cellule squamose e il carcinoma a grandi cellule. 2
Esistono tuttavia numerose altre tipi di NSCLC, che sono meno frequenti. 1

ADENOCARCINOMA
Costituisce la forma di NSCLC più comune 1 e rappresenta il 40% di tutti i tumori polmonari maligni. 4 Ha origine dalle cellule secernenti muco che rivestono la superficie interna delle vie respiratorie, 3 solitamente nel tessuto polmonare periferico. 1
Si verifica prevalentemente tra i fumatori, nelle donne e rappresenta il tumore polmonare più frequente nella popolazione giovane. 2
CARCINOMA A CELLULE SQUAMOSE
Costituisce il 25-30% di tutti i tumori polmonari, 4 ha origine a livello delle cellule che rivestono le vie respiratorie e tende a crescere al centro del polmone. 3 È più frequente tra i fumatori. 2
CARCINOMA A GRANDI CELLULE
Rappresenta il 10-15% di tutti i tumori polmonari e prende il nome dall’aspetto al microscopio delle cellule che lo compongono. 4
Può insorgere in qualsiasi area del polmone e tende a crescere rapidamente. 2
Bibliografia
- General Information About Non-Small Cell Lung Cancer (NSCLC). National Cancer Institute (NIH). Disponibile al sito: https://www.cancer.gov/types/lung/hp/non-small-cell-lung-treatment-pdq
- What is lung cancer. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/cancer/lung-cancer/about/what-is.html
- Types of lung cancer. Cancer Research UK. Disponibile al sito: https://www.cancerresearchuk.org/about-cancer/lung-cancer/stages-types-grades/types
- Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
Come in molti altri ambiti, non esiste un unico trattamento per il tumore al polmone; questo dipende infatti dallo stadio, dalla mutazione che il cancro al polmone presenta e anche dal paziente. È giusto infatti che a ogni paziente sia chiesta un’opinione su quale trattamento preferisce. 1
In alcuni casi, inoltre, il medico decide di procedere con più di un trattamento, combinandoli per renderli più efficaci. 1
PRINCIPALI TRATTAMENTI A DISPOSIZIONE PER IL TUMORE AL POLMONE IN FASE INIZIALE1
Intervento chirurgico: indicato per l’NSCLC in stadio iniziale. Ci sono 3 modalità diverse con cui si interviene:
- rimuovendo una parte molto piccola del polmone, l’intervento viene chiamato resezione segmentaria;
- rimuovendo una parte maggiore e delimitata del polmone (detta lobo), da qui il nome lobectomia;
- rimuovendo l’intero polmone, in questo caso si parla di pneumonectomia.
Chemioterapia: si tratta il tumore con farmaci che uccidono le cellule tumorali. La chemioterapia può essere fatta prima dell’intervento chirurgico, per diminuire le dimensioni del tumore, o subito dopo1 per eradicare l’eventuale presenza ancora di malattia o prevenire eventuali successive ricadute.2
Radioterapia: grazie a radiazioni ad elevata energia (ionizzanti) si danneggiano le cellule tumorali così da causarne la morte. Può essere utilizzata per trattare il tumore al polmone sia in stadio precoce, sia in stadio più avanzato.1
Chemioradioterapia: è un trattamento combinato che consiste nel ricevere contemporaneamente chemio e radioterapia.1
Ci sono poi trattamenti più innovativi e probabilmente meno universalmente noti, che però stanno dando ottimi risultati:1
- Le cosiddette terapie a bersaglio molecolare: hanno lo stesso scopo della chemioterapia, cioè eliminare le cellule tumorali, ma lo fanno in maniera specifica, legandosi cioè direttamente a una parte della cellula tumorale, così da non colpire le cellule sane circostanti, cosa che invece succede con la chemioterapia.
- Le terapie anti-angiogeniche: il loro scopo è impedire al tumore di formare nuovi vasi sanguigni, che gli servono per crescere di dimensione e per espandersi.
- L’immunoterapia: i tumori sono in grado di «nascondersi» al sistema immunitario tramite diversi meccanismi. L’immunoterapia blocca questi meccanismi così che il sistema immunitario possa attivarsi per combattere il tumore.
BIBLIOGRAFIA
- Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
- How Is Chemotherapy Used to Treat Cancer? American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/treatment/treatments-and-side-effects/treatment-types/chemotherapy/how-is-chemotherapy-used-to-treat-cancer.html
