I numeri della malattia
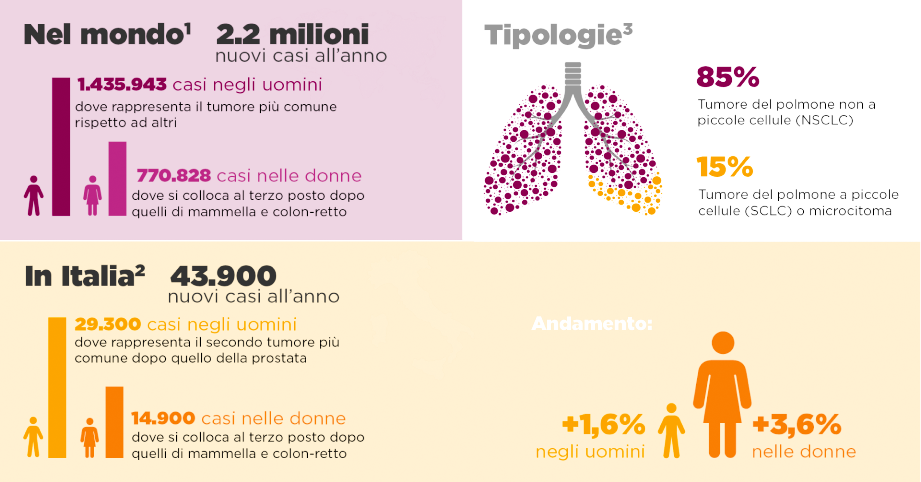
Il tumore del polmone rappresenta oggi il secondo tumore più frequente a livello globale dopo quello della mammella, mentre in Italia è il terzo tumore dopo quello della mammella e quello del colon-retto.1,2
L’incidenza è in crescita nei paesi in via di sviluppo, in molti dei quali si registra un incremento nella percentuale di fumatori.3
Polmone: un solo organo, tante malattie
Una tosse che non passa, il fiato corto, una stanchezza che non si spiega. Sono solo alcuni dei sintomi che possono far pensare a un tumore del polmone, ma sono anche sintomi molto generici, che potrebbero essere causati da problemi che con il tumore non hanno niente a che fare. Per questa ragione è importante, in presenza di sintomi sospetti rivolgersi al proprio medico che, con l’aiuto dello specialista, potrà dare il via al percorso di diagnosi più adatto a ciascun caso.4
Come si arriva alla diagnosi? Il primo passo è senza dubbio il colloquio con il medico che valuta la storia clinica e i sintomi ed esegue una visita completa. Seguono una serie di esami cosiddetti di “diagnostica per immagine” (raggi X, TC, PET, risonanza magnetica) mirati a identificare la presenza del tumoree la sua estensione nell’organismo. Da lì si prosegue con esami che valutano il buon funzionamento dei polmoni e con un prelievo di un campione di cellule o di tessuto (biopsia) che verrà in seguito analizzato in laboratorio.4 E per la diagnosi precoce della malattia sono in fase di studio anche in Italia programmi di screening mirato nelle popolazioni più a rischio.5
Attenzione però. Parlare di tumore del polmone al singolare è riduttivo. Oltre ai due tipi principali – NSCLC e SCLC – sono stati identificati numerosi sottogruppi della malattia in base alla presenza di specifiche alterazioni molecolari, che possono variare da paziente a paziente, ma anche nello stesso paziente nel corso del tempo. Identificare tali alterazioni attraverso test molecolari specifici significa ottenere una fotografia più accurata della malattia e un aiuto nella scelta della terapia.6 Infine, anche la presenza di specifiche caratteristiche immunitarie del tumore e dell’ambiente che lo circonda possono influenzare le successive scelte terapeutiche.7
Percorsi di cura personalizzati e innovativi
Il tumore del polmone non è un’unica malattia e di conseguenza non è possibile parlare di un unico trattamento adatto a tutti i pazienti senza distinzione. Come succede anche in altri tumori, infatti, nel tumore del polmone la scelta del percorso terapeutico dipende dalle caratteristiche del paziente, ma anche dal tipo di malattia con la quale ci si confronta.8
La chirurgia rappresenta la prima scelta nei casi di tumore in fase precoce. Anche la radioterapia può avere un ruolo in diversi momenti del trattamento del tumore del polmone: ad esempio in associazione alla chemioterapia in tumori localmente avanzati, oppure a scopo palliativo, per alleviare i sintomi del tumore.4
Accanto a queste tecniche più tradizionali, sono oggi disponibili per i pazienti numerose alternative per personalizzare la terapia.
Si parte dalle terapie a bersaglio molecolare o targeted therapy. Si tratta di classi di farmaci diretti contro geni che risultano alterati in quello specifico tumore ed efficaci anche nei pazienti con malattia avanzata o metastatica. Negli ultimi due decenni – è del 2005 l’approvazione europea del primo di questi trattamenti9 – lo sviluppo delle tecniche per ottenere i profili molecolari e l’arrivo di queste nuove terapie hanno aperto la strada alla medicina di precisione, soprattutto per il NSCLC in fase avanzata.10
A completare il quadro, da qualche anno si è affacciata all’orizzonte anche l’immunoterapia che sta modificando profondamente l’approccio al trattamento del cancro, grazie al suo profilo di tollerabilità, alla risposta mantenuta nel tempo e all’efficacia in un ampio gruppo di pazienti.11
La chirurgia non è tutto!
Fino a pochi anni fa la diagnosi di un tumore “non resecabile”, ovvero che non può essere asportato con la chirurgia, si traduceva in una drastica riduzione delle possibilità di intervenire in modo efficace e il trattamento standard di chemio-radioterapia non portava a risultati particolarmente soddisfacenti.12
Ma oggi la situazione è molto diversa e l’introduzione di terapie innovative ha cambiato le carte in tavola, offrendo una prospettiva di cura per i pazienti con malattia in stadio localmente avanzato (stadio III) non resecabile.13
Oggi l’immunoterapia è entrata a pieno diritto in questo contesto e ha acceso una nuova luce per i pazienti con tumore non operabile.12 In particolare, gli inibitori di PD-L1 possono essere oggi utilizzati come terapia di consolidamento, e riescono a bloccare in modo efficace la progressione della malattia.4
I numerosi studi oggi in corso mostrano risultati incoraggianti che vanno verso un aumento del numero di persone che possono beneficiare dell’immunoterapia e, potenzialmente, potranno accedere a una possibilità di cura.13
E se il tumore è resecabile? Anche in questo caso non è detto che la chirurgia da sola sia sufficiente. In particolare, per eliminare eventuali cellule non asportate con il bisturi e ridurre così il rischio che il tumore ritorni si utilizza la cosiddetta terapia adiuvante, ovvero la terapia somministrata dopo l’intervento chirurgico, che può essere proposta ai pazienti con malattia localmente avanzata (stadio III) ma anche a quelli con tumore in stadio più precoce (anche in stadio I). Per quanto riguarda la scelta della terapia adiuvante, i medici hanno a disposizione diverse opzioni, da sole o in combinazione: dalla radioterapia alla chemioterapia, per arrivare alle terapie a bersaglio molecolare e all’immunoterapia. Il tutto ancora una volta disegnato su misura per il singolo paziente.4

Obiettivo qualità di vita
Curare un paziente non significa solo cercare il trattamento più efficace contro la sua malattia, ma richiede un impegno a 360 gradi che includa tutti i reali bisogni della persona e tenga conto della qualità di vita. Si tratta di valutare l’esperienza di malattia, così come il singolo paziente la vive e non solo di osservare l’efficacia di un trattamento.14
Entrano allora in gioco i cosiddetti patient reported outcomes (PRO), ovvero gli esiti riportati direttamente dai pazienti, che negli ultimi anni hanno guadagnato sempre più spazio nell’oncologia clinica e come strumento per misurare la qualità di vita, un parametro che oggi è parte integrante della ricerca clinica, epidemiologica e di economia sanitaria.15
Da non dimenticare il fatto che una migliore qualità di vita influenza in modo positivo anche la sopravvivenza dei pazienti oncologici, inclusi quelli con tumore del polmone.16
Usati nel modo corretto, questi strumenti possono davvero fare la differenza.
©AstraZeneca – Codice IT-10928 – Data di approvazione: 27/10/2023
BIBLIOGRAFIA
- IARC-WHO. Global Cancer observatory. https://gco.iarc.fr/ [Ultimo accesso 17 settembre 2023]
- AIOM, AIRTUM, et al. I numeri del cancro in Italia 2022
- Leiter A, Veluswamy RR, Wisnivesky JP. The global burden of lung cancer: current status and future trends. Nat Rev Clin Oncol. 2023;20(9):624-639. doi:10.1038/s41571-023-00798-3
- American Cancer Society – Lung Cancer. https://www.cancer.org/cancer/types/lung-cancer.html [Ultimo accesso 17 settembre 2023]
- Ministero della Salute. La diagnosi precoce del tumore del polmone – La Rete italiana screening polmonare (RISP). [Aggiornamento 7 febbraio 2023]
- Zito Marino F, Bianco R, Accardo M, et al. Molecular heterogeneity in lung cancer: from mechanisms of origin to clinical implications. Int J Med Sci. 2019;16(7):981-989. Published 2019 Jun 10. doi:10.7150/ijms.34739
- Lv X, Mao Z, Sun X, Liu B. Intratumoral Heterogeneity in Lung Cancer. Cancers (Basel). 2023;15(10):2709. Published 2023 May 11. doi:10.3390/cancers15102709
- ESMO For patients. Personalised Medicine at a Glance: Lung Cancer. [updated in February 2017]
- Steeghs EMP, Groen HJM, Schuuring E, et al. Mutation-tailored treatment selection in non-small cell lung cancer patients in daily clinical practice. Lung Cancer. 2022;167:87-97. doi:10.1016/j.lungcan.2022.04.001
- Hofmarcher T, Malmberg C, Lindgren P. A global analysis of the value of precision medicine in oncology – The case of non-small cell lung cancer. Front Med (Lausanne). 2023;10:1119506. Published 2023 Feb 20. doi:10.3389/fmed.2023.1119506
- Lahiri A, Maji A, Potdar PD, et al. Lung cancer immunotherapy: progress, pitfalls, and promises. Mol Cancer. 2023;22(1):40. Published 2023 Feb 21. doi:10.1186/s12943-023-01740-y
- Remon J, Hendriks LEL. Targeted therapies for unresectable stage III non-small cell lung cancer. Mediastinum. 2021;5:22. Published 2021 Sep 25. doi:10.21037/med-21-8
- Cortiula F, Reymen B, Peters S, et al. Immunotherapy in unresectable stage III non-small-cell lung cancer: state of the art and novel therapeutic approaches. Ann Oncol. 2022;33(9):893-908. doi:10.1016/j.annonc.2022.06.013
- Koller M, Shamieh O, Hjermstad MJ, et al. Psychometric properties of the updated EORTC module for assessing quality of life in patients with lung cancer (QLQ-LC29): an international, observational field study. Lancet Oncol. 2020;21(5):723-732. doi:10.1016/S1470-2045(20)30093-0
- Hechtner M, Eichler M, Wehler B, et al. Quality of Life in NSCLC Survivors – A Multicenter Cross-Sectional Study. J Thorac Oncol. 2019;14(3):420-435. doi:10.1016/j.jtho.2018.11.019
- Hong YJ, Han S, Lim JU, et al. Association Between Quality of Life Questionnaire at Diagnosis and Survival in Patients With Lung Cancer. Clin Lung Cancer. 2023;24(5):459-466. doi:10.1016/j.cllc.2023.03.007

Permessi1
Chi presta assistenza a un paziente con disabilità grave ha diritto
a 3 giorni di permesso mensile, frazionabili in ore.

Congedo non retribuito di due anni1
In caso di gravi motivi familiari (decessi, malattie gravi di familiari), è possibile usufruire di un congedo non retribuito di due anni, continuativo o frazionato.


Congedo retribuito di due anni1
In caso di necessità di assistenza di un familiare con disabilità, è possibile usufruire di un congedo retribuito di due anni (che degrada solo in caso di mancanza, decesso o in presenza di patologie invalidanti dei primi).
Ne hanno diritto secondo un ordine di priorità:
- coniuge o partner dell’unione civile convivente
- padre o madre, anche adottivi o affidatari
- figlio convivente
- fratello o sorella convivente
- parente o affine entro il terzo grado convivente
- figlio non ancora convivente (che instauri la convivenza entro l’inizio del periodo di congedo richiesto)
BIBLIOGRAFIA
- Diritti e tutele in caso di malattie oncologiche. Disponibile al sito: https://www.inps.it/docallegatiNP/Mig/AllegatiNews/Diritti_e_tutele_malattie_oncologiche.pdf
Assegno mensile di invalidità civile1
A CHI È RIVOLTO
Invalidi parziali di età compresa tra i 18 e i 67 anni, con una riduzione della capacità lavorativa compresa tra il 74 e il 99%, reddito entro i limiti personali stabiliti annualmente e il non svolgimento di attività lavorativa (salvo casi particolari).
INCOMPATIBILITÀ
È incompatibile con qualsiasi pensione diretta di invalidità erogata
a qualsiasi titolo dall’INAIL e con qualsiasi pensione di invalidità erogata a qualsiasi titolo dall’Assicurazione Generale Obbligatoria e da altri enti a lavoratori dipendenti o autonomi. L’interessato può optare per il trattamento economico
più favorevole.
Pensione di inabilità per invalidi civili1
A CHI È RIVOLTA
Invalidi totali di età compresa tra i 18 e i 67 anni in stato di bisogno economico.
COMPATIBILITÀ
È compatibile con lo svolgimento di attività lavorativa e con le prestazioni erogate a titolo di invalidità per causa
di guerra, di lavoro o di servizio.
Indennità di accompagnamento1
A CHI È RIVOLTA
Persone con totale inabilità per le quali è stata accertata l’impossibilità di deambulare senza l’aiuto di un accompagnatore o l’incapacità di compiere gli atti quotidiani della vita, indipendentemente dal personale annuo e dall’età.
COMPATIBILITÀ
È compatibile con lo svolgimento di attività lavorativa.
BIBLIOGRAFIA
- Diritti e tutele in caso di malattie oncologiche. Disponibile al sito: https://www.inps.it/docallegatiNP/Mig/AllegatiNews/Diritti_e_tutele_malattie_oncologiche.pdf

Esenzione ticket1
- In presenza di malattia oncologica si ha diritto all’esenzione totale dal ticket per prestazioni sanitarie necessarie al monitoraggio della patologia, visite specialistiche, esami di laboratorio, strumentali o diagnostici e per l’acquisto di farmaci.
- In caso di invalidità del 100% si ha diritto all’esenzione totale dal pagamento per farmaci e visite per qualunque patologia.


Contrassegno e altre agevolazioni1:
È possibile usufruire di altri diritti se previsti espressamente nel verbale di riconoscimento dell’invalidità, quali:
- contrassegno disabili
- detrazioni per figli a carico
- detrazioni per le spese mediche
- assistenza personale per chi non è autosufficiente
- IVA agevolata su ausili tecnici e informatici
- agevolazioni per non vedenti
- agevolazioni sulle ristrutturazioni per eliminare barriere architettoniche
- agevolazioni sull’acquisto dell’auto
- calcolo dell’imposta di successione e donazioni con aliquote differenti.
BIBLIOGRAFIA
- Diritti e tutele in caso di malattie oncologiche. Disponibile al sito: https://www.inps.it/docallegatiNP/Mig/AllegatiNews/Diritti_e_tutele_malattie_oncologiche.pdf
Il riconoscimento dello status di invalido civile (legge 104/1992) permette di accedere alle misure
di assistenza di tipo economica (pensioni, assegni, indennità), e non economica (assistenza sanitaria, agevolazioni sul lavoro, ecc.), secondo i principi della Costituzione italiana.1

Come fare la domanda di invalidità civile2

Certificato medico2
Il primo passaggio consiste nel richiedere al proprio medico curante il certificato medico introduttivo, che attesti la natura della patologia invalidante. Il medico provvede a inoltrare telematicamente il certificato alla struttura territoriale INPS e a consegnarvi:
- una ricevuta con un codice identificativo
- una copia del certificato medico originale.

Domanda all’INPS2
Una volta ottenuto il certificato medico è possibile presentare la domanda all’INPS esclusivamente per via telematica:
- direttamente dal sito www.inps.it
- tramite gli enti di patronato o le associazioni di categoria dei disabili.

Accertamento agli atti2
Le domande di accertamento presentate dai malati oncologici possono essere validate senza necessità di effettuare l’accertamento sanitario in presenza. Tale modalità, anche per effetto dell’emergenza sanitaria in atto, è diventata ormai ordinaria in tutti i casi nei quali è possibile evitare l’accertamento in presenza.

Aggravamento2
Anche in corso di sottomissione della domanda, per i malati oncologici è sempre possibile presentare una nuova domanda di aggravamento.

Iter accelerato per malati oncologici2
In caso di malattia oncologica, la visita deve effettuarsi entro 15 giorni dalla domanda e gli esiti sono immediatamente produttivi dei benefici che da essi conseguono.
BIBLIOGRAFIA
- Portale INPS. Disponibile al sito: https://www.inps.it/nuovoportaleinps/default.aspx?itemdir=49810
- Diritti e tutele in caso di malattie oncologiche. Disponibile al sito: https://www.inps.it/docallegatiNP/Mig/AllegatiNews/Diritti_e_tutele_malattie_oncologiche.pdf

Periodo di comporto1:
Durante l’assenza dal lavoro per malattia oncologica è garantito il diritto alla conservazione del posto di lavoro per il periodo cosiddetto di comporto.

Visita fiscale1:
In caso di terapie salvavita (tra cui le cure chemioterapiche) non è richiesto il rispetto degli orari di reperibilità per la visita fiscale che può essere eseguita solo previo accordo con il lavoratore.


Permessi1:
I pazienti oncologici con disabilità grave hanno diritto a:
- 3 giorni di permesso mensile, frazionabili in ore
- 2 ore al giorno (1, se l’orario di lavoro è inferiore a 6 ore)

Congedi1:
In caso di riconoscimento dell’invalidità civile >50%, è possibile usufruire di un congedo per cure fino a 30 giorni all’anno.

Collocamento obbligatorio1:
In caso di riconoscimento dell’invalidità civile >45% si ha diritto all’iscrizione nelle liste speciali del collocamento. Tutti i datori di lavoro, pubblici e privati, con più di 15 dipendenti hanno l’obbligo di assunzione per questi soggetti.
BIBLIOGRAFIA
- Diritti e tutele in caso di malattie oncologiche. Disponibile al sito: https://www.inps.it/docallegatiNP/Mig/AllegatiNews/Diritti_e_tutele_malattie_oncologiche.pdf
È l’insieme di trattamenti che aiutano a migliorare la vita di tutti i giorni e provano a contrastare dolori e sofferenze derivanti dalla convivenza con il tumore al polmone.1
Sentirsi sopraffatti dai trattamenti è normale e ricevere aiuto è un diritto fondamentale (legge 38/2010).1
Il nome «cure palliative» racchiude sia i farmaci somministrati che l’insieme dei professionisti i cui sforzi mirano sì a contrastare il dolore ma anche ad attenuare i diversi sintomi della malattia tra cui i problemi di respirazione e la perdita di appetito.1
Tali cure non mirano a curare la malattia, non sempre infatti si riesce a curare il tumore al polmone, ma puntano a far stare bene la persona, a migliorare ogni piccolo aspetto della sua quotidianità, durante e dopo il trattamento (radioterapico, chemioterapico ecc). 1
Non va inoltre dimenticato l’aspetto psicologico; il tumore al polmone è una malattia sfidante per chi la vive in prima persona e per chi lo circonda ed è fondamentale non trascurare le ripercussioni che si possono avere sull’aspetto psicologico. Nell’ambito delle cure palliative non mancano infatti la psicoterapia e il counselling sia individuale che familiare.1
HOSPICE
Non sempre si ha a disposizione un luogo in cui vivere la propria malattia in modo sereno, con le necessità che il tumore al polmone porta con sé c’è bisogno di strutture adatte, professionisti competenti e strumenti adeguati e non sempre si riesce ad avere tutte queste cose nella propria casa.2
È per tale motivo che sono nati gli hospice, centri residenziali per persone affette da patologie che richiedono assistenza continua, cure adeguate e una struttura in grado di accogliere non solo il paziente in prima persona ma anche i suoi familiari.2
Gli hospice sono dotati di personale medico, infermieristico, di tutte le figure che orbitano nell’universo sanità (fisioterapista, psicologo, radiologo…) e permettono alla persona affetta da tumore al polmone di avere un’assistenza adeguata in una struttura all’altezza delle sue nuove esigenze, senza sentire il distacco dalla famiglia.2

BIBLIOGRAFIA
- Sito web AIOT – AIOTOWN, 7. Cure palliative – A. Cosa sono le cure palliative
- Sito web AIOT – AIOTOWN, 7. Cure palliative – C. Hospice
STADI DI MALATTIA
Lo stadio del tumore può essere valutato in due modi:1
- Sistema TNM: valuta le dimensioni del tumore primario (T), se ci sono infiltrazioni del tumore nei linfonodi (N) e la presenza o meno di metastasi (M).1 Permette di caratterizzare in maniera più accurata e dettagliata la patologia e le dimensioni della massa.
- Classificazione della malattia in stadio limitato (malattia presente solo in una metà del torace, verosimilmente in un solo polmone) e in stadio esteso (presenza di metastasi in altri organi o tessuti). Utilizzata più comunemente e permette all’oncologo di indirizzare il paziente alla terapia più adatta in modo più rapido. A ciascuno dei due stadi, limitato ed esteso, corrisponde infatti una specifica strategia terapeutica.

BIBLIOGRAFIA
- Sito web AIOT – AIOTOWN, 2. Storia della malattia – C. Stadiazione
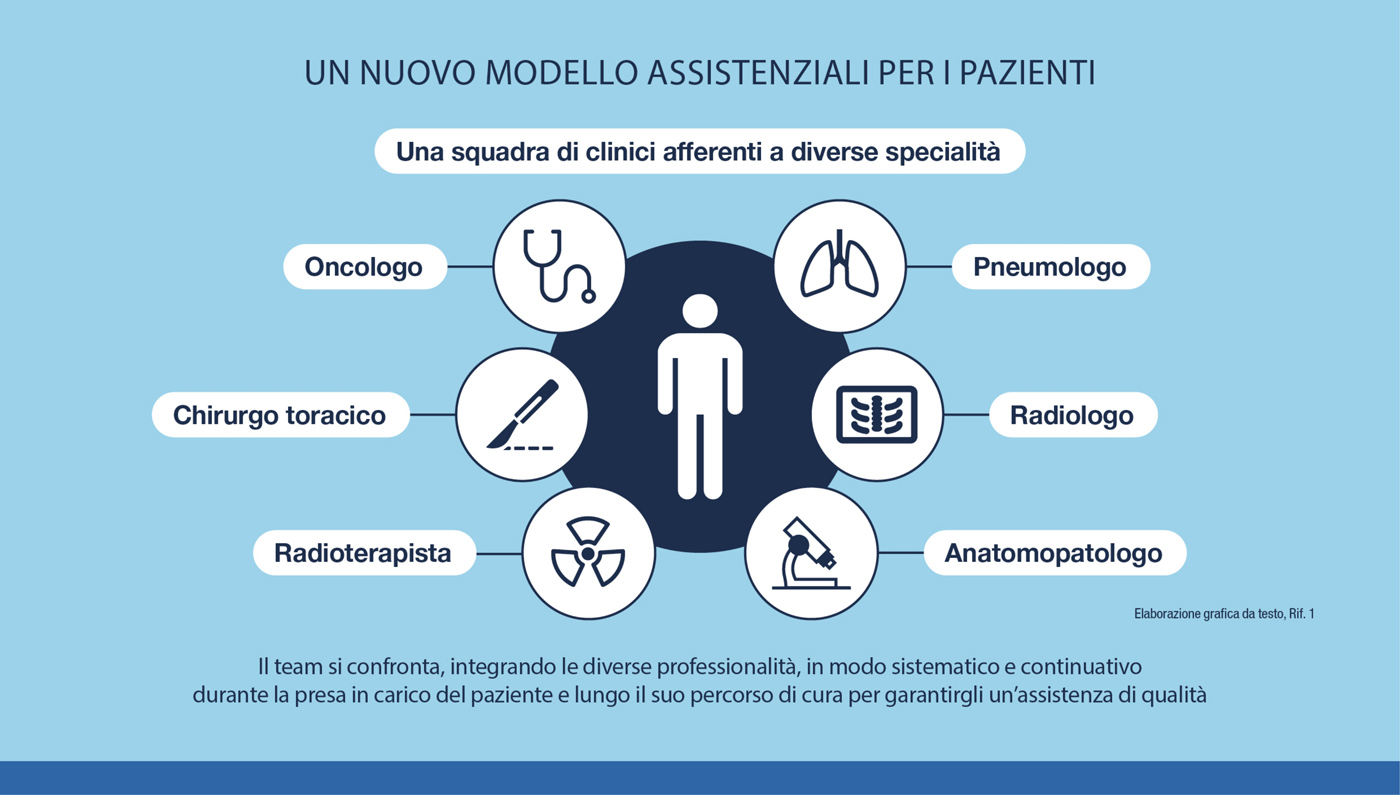
La gestione del carcinoma polmonare richiede la partecipazione di diverse figure specializzate per assicurare una cura ottimale al paziente, per questo è importante la presenza di un team multidisciplinare. 1
Diversi studi hanno analizzato l’impatto positivo del team multidisciplinare su numerosi parametri.
In particolare, uno studio condotto su >4000 pazienti ha dimostrato che:2
- la diagnosi e il trattamento del tumore al polmone gestiti da un team multidisciplinare si traduce in un significativo beneficio in termini di sopravvivenza.
Inoltre, l’applicazione del modello del team multidisciplinare permette il superamento di barriere relative ai trattamenti, promuove la prescrizione di terapie standardizzate attraverso l’aderenza alle linee guida e per queste ragioni fornisce un’assistenza di qualità per i pazienti con carcinoma polmonare3.
BIBLIOGRAFIA
- Prabhakar CN et al, Respirology, 20 (6), 884-8
- Bilifinger TV, et al. Clin Lung Cancer. 2018 Jul;19(4):346-351
- Denton E, et al. J Multidiscip Healthc. 2016;9:137-44
Elaborazione grafica da testo, Rif. 1
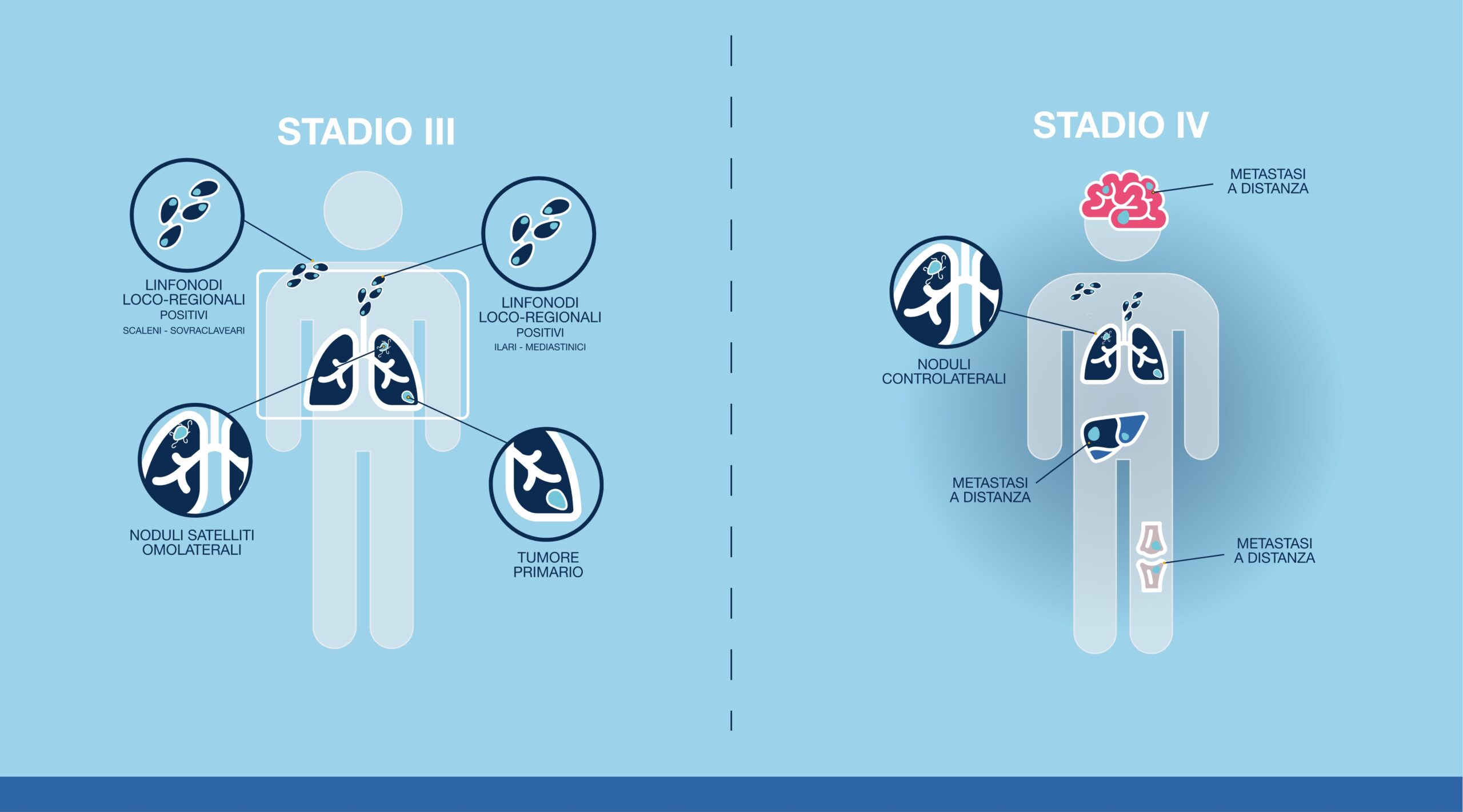
Lo stadio del tumore è definito da diverse caratteristiche fisiologiche: 1

STADIO III
Il tumore si può presentare con diverse combinazioni delle tre caratteristiche citate; la sua dimensione può essere variabile e iniziano a essere coinvolti i linfonodi loco-regionali più o meno lontani. Nello stadio III il tumore è ancora localizzato all’interno del torace.
STADIO IV
Il tumore ha iniziato la sua diffusione, si ritrovano quindi metastasi in altri organi. Nello stadio IV è possibile che siano presenti metastasi in un solo organo (ad esempio il cervello) o in più organi contemporaneamente (ad esempio cervello, ossa, fegato, ecc…)
BIBLIOGRAFIA
- AIOM Linee Guida NEOPLASIE DEL POLMONE. Edizione 2018.
SOMMINISTRAZIONE: 1
Gli immunoterapici vengono tutti somministrati per infusione endovenosa, con uno schema preciso in base al tipo di trattamento.
Per l’infusione è sempre necessario andare in ospedale e la somministrazione del farmaco dura circa un’ora e mezza.
EFFETTI COLLATERALI: 1
Gli effetti collaterali dell’immunoterapia sono differenti rispetto a quelli provocati dalle altre terapie contro il cancro. Non tutti i pazienti sperimentano lo stesso tipo di effetti collaterali e alcune persone potrebbero non averne affatto. In genere, gli effetti collaterali compaiono entro poche settimane o mesi dall’inizio della terapia, ma possono insorgere in qualsiasi momento.
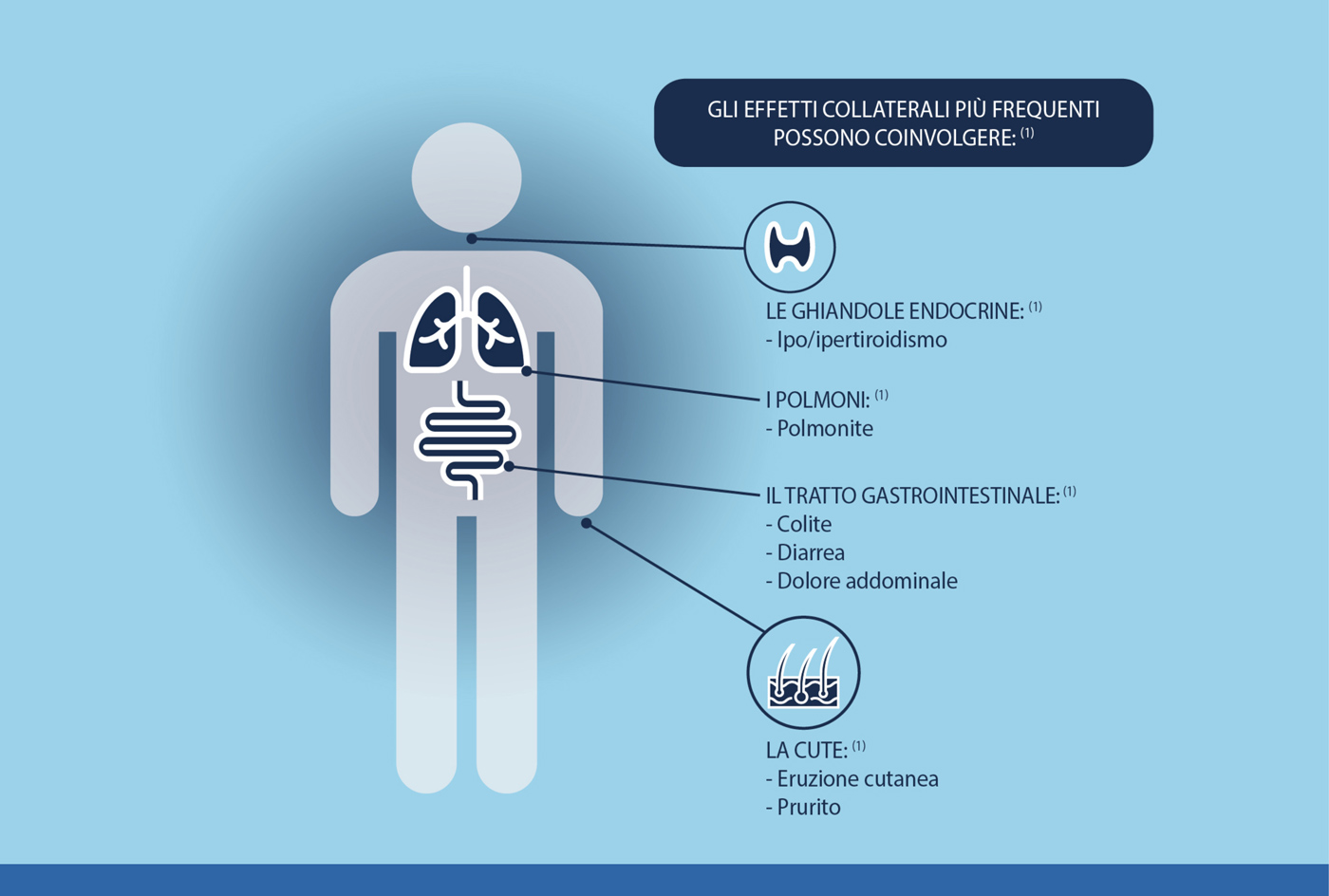
L’importanza della comunicazione 1
- Una corretta informazione è fondamentale per il riconoscimento e la segnalazione precoce dei segni e sintomi degli effetti collaterali.
- La comunicazione diretta e la stretta interazione tra paziente, oncologo e medico di medicina generale, rendono il trattamento più sicuro, gestibile ed efficace.
- Per il paziente, sapere cosa aspettarsi e come prevenire o gestire gli effetti collaterali può essere d’aiuto per mantenere sotto controllo la situazione e per migliorare la qualità della vita.
Consigli per la vita quotidiana 1
- Chiedi al tuo oncologo tutto quello che desideri sapere a proposito della malattia.
- Fai attività fisica, l’esercizio aiuta a contrastare la stanchezza e favorisce l’appetito.
- Segui una dieta sana.
- Tieni un diario quotidiano del trattamento, scrivendo come ti senti e cosa pensi.
- Ascolta sempre il tuo corpo.
BIBLIOGRAFIA
- Di Giacomi AM, Maio M, Monterisi S. Immunoterapia. Cosa tenere sotto controllo. Una guida pratica per il paziente. Effetti Editore, 2019
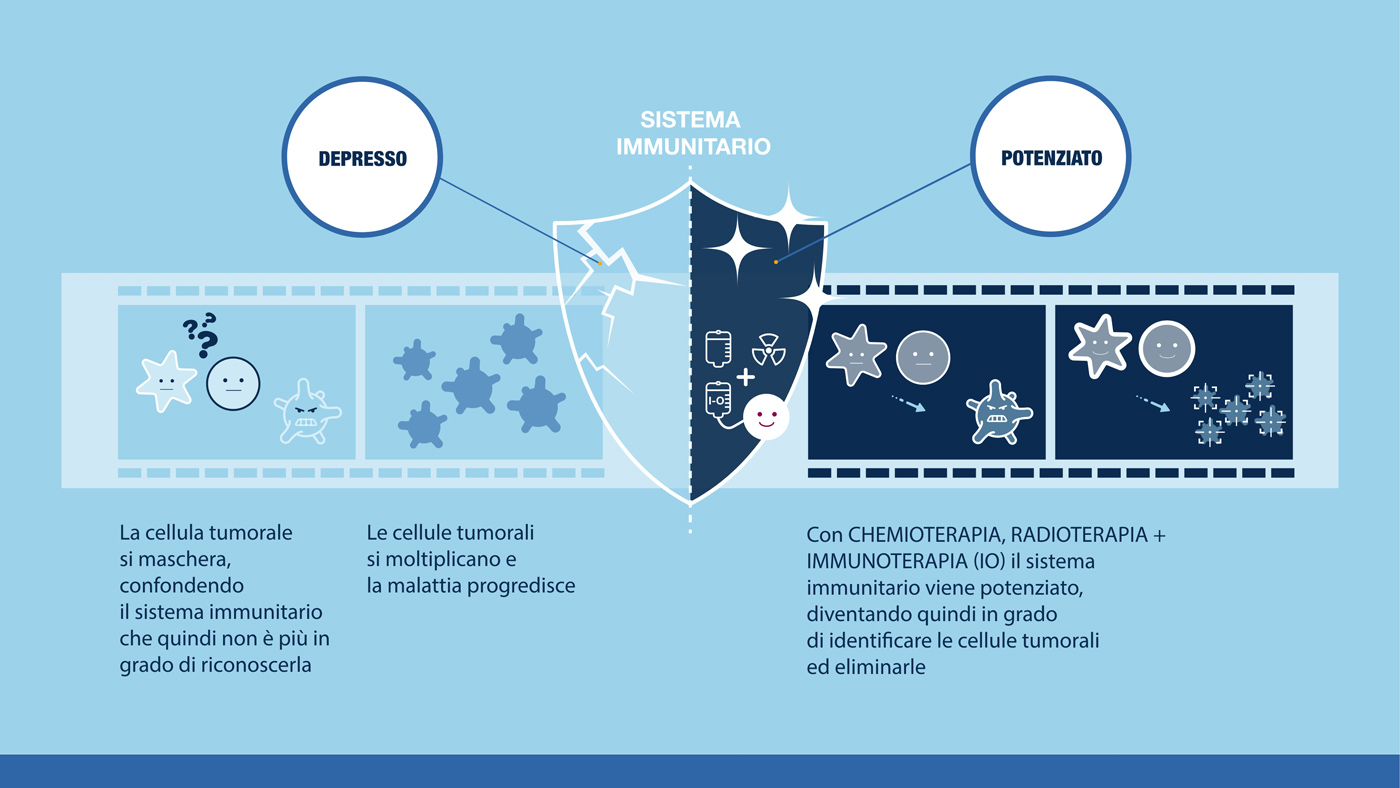
Le cellule tumorali eludono il sistema immunitario mascherandosi e inibendo la risposta difensiva, in questo modo sono in grado di moltiplicarsi in modo incontrollato.1
L’immuno-oncologia non colpisce direttamente le cellule tumorali ma attiva le cellule del sistema immunitario, mettendole nelle condizioni di distruggere il tumore.1 Così facendo impedisce alle cellule malate di sfuggire al controllo del sistema immunitario e mantiene i meccanismi di difesa sempre attivi.1
BIBLIOGRAFIA
- Mauro Boldrini, Sabrina Smererei, Paolo Cabra. Immuno-oncologia. 100 domande 100 risposte. La guida per conoscere la nuova arma contro i tumori e il “pianeta” cancro. Seconda edizione. AIOM.
Ogni tumore è differente e, sulla base dello stadio in cui la malattia si trova, ha bisogno di un diverso tipo di trattamento o di una diversa combinazione di trattamenti.
STADIO I E II
Lo stadio I e II definisce lo stadio iniziale della malattia, non esteso a nessun’altra parte del corpo e di piccole dimensioni, quindi potenzialmente curabile con l’intervento chirurgico. 1
In base alla presenza o meno delle cellule nei linfonodi circostanti il tumore, prelevati durante l’intervento per essere analizzati, si decide se, in seguito all’intervento, è opportuno un trattamento definito «adiuvante» con chemioterapia o radioterapia. 1
STADIO III
Lo stadio III definisce il tumore in stadio avanzato, ma non ancora diffuso in altre parti del corpo. Nello stadio III sono compresi tumori che non presentano cellule tumorali all’interno dei linfonodi, tumori positivi per un numero limitato di linfonodi e tumori con un numero importante di linfonodi coinvolti.1 In base a queste tre caratteristiche, viene identificata la terapia più adeguata: 1
- Se il tumore è considerato operabile si procede con l’intervento chirurgico, preceduto o seguito da chemioterapia e/o da radioterapia.
- Se la chirurgia inizialmente è controindicata perché, ad esempio, la massa è troppo estesa o la posizione è complicata da raggiungere, si interviene con una combinazione di chemio e radioterapia «neo-adiuvante» e, solo in un secondo momento, si considera l’intervento chirurgico.
- Se il tumore è non operabile e quindi l’intervento è da scartare, si procede con il trattamento a base di chemioterapia e radioterapia, anche somministrate contemporaneamente.
Nei pazienti in cui non è possibile procedere con l’intervento chirurgico, nel caso in cui il tumore torni a crescere e ad espandersi dopo trattamenti chemioterapico/radioterapico, si può procedere con l’immunoterapia. 1
STADIO IV
Lo stadio IV definisce una malattia metastatica, cioè diffusa ad altre parti del corpo oltre al polmone.1 In questo caso l’intervento chirurgico non può essere considerato e l’opzione di trattamento preferenziale è la terapia farmacologica che varia in base alle caratteristiche molecolari specifiche del tumore:1
- In assenza di mutazioni genetiche o con bassi livelli di PD-L1 = chemioterapia
- In presenza di mutazioni EGFR, BRAF, ALK o ROS1 = terapie a bersaglio molecolare
- In presenza di elevati livelli di proteina PD-L1 = immunoterapia.
BIBLIOGRAFIA
- Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
Il fumo è uno dei fattori di rischio più importanti per il tumore al polmone e il principale per lo sviluppo del SCLC; 1 non solo è in grado di aumentare il rischio di ammalarsi di tumore al polmone ma rende anche le cellule tumorali più aggressive e resistenti ai farmaci chemioterapici. 2

Uno dei modi per prevenire l’insorgenza di un tumore al polmone è smettere di fumare il prima possibile così da abbassare la probabilità di ammalarsi. Bisogna inoltre prestare attenzione a non inalare il fumo passivo dai fumatori che ci circondano. Non importa per quanto tempo si è fumato in precedenza, smettere può comunque diminuire le probabilità di sviluppare un tumore al polmone. 1
In questi ultimi anni si è poi assistito al proliferare dei cosiddetti sistemi elettronici di erogazione della nicotina (Electronic Nicotine Delivery Systems, ENDS) che comprendono le sigarette elettroniche, i dispositivi per lo svapo, i narghilè, le pipe e i sigari, tutti elettronici. Ci sono poi i prodotti “heat not burn” che scaldano il tabacco ad elevate temperature senza però che esso bruci.3 Tutti questi surrogati del fumo non hanno ancora una diretta correlazione con l’insorgenza di un tumore al polmone ma sono ben lungi dall’essere considerati “non a rischio”. Inoltre, è stato dimostrato come coloro i quali si dotano di tutti questi dispositivi sono più propensi a tornare o ad iniziare a fumare la classica sigaretta. 4
Anche evitare l’esposizione ad agenti cancerogeni aiuta a prevenire l’insorgenza della malattia. Sui luoghi di lavoro si è normalmente tutelati dalle leggi sulla sicurezza nei luoghi di lavoro e, nella vita di tutti i giorni, basta evitare di esporsi a sostanze chimiche di cui non si conosce la pericolosità. 1
I ricercatori hanno poi osservato come coloro che bruciano carbone e biomasse quali legna, ramoscelli e residui di coltivazioni sia per cucinare che per scaldarsi, hanno un aumento del rischio di ammalarsi di tumore al polmone. Il carbone bruciato a livello domestico è stato quindi classificato come cancerogeno. 4
Ci sono infine le raccomandazioni più di carattere generale che valgono per condurre una vita sana ma che, indirettamente, ci aiutano a ridurre il rischio: avere uno stile di vita sano, adottando un’alimentazione equilibrata composta da frutta e verdura. 1
Bibliografia
- Can Lung Cancer Be Prevented? American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/cancer/lung-cancer/causes-risks-prevention/prevention.html#written_by
- Cataldo J, et al. Smoking cessation: an integral part of lung cancer treatment. Oncology 2010;78:289–301. https://pubmed.ncbi.nlm.nih.gov/20699622/
- Sigarette elettroniche, prodotti a tabacco riscaldato non bruciato e senza fumo. European Lung Foundation (ELF). Disponibile al sito: https://europeanlung.org/it/information-hub/factsheets/sigarette-elettroniche-prodotti-a-tabacco-riscaldato-non-bruciato-e-senza-fumo/
- Bade CB, Dela Cruz CS. Lung cancer 2020: epidemiology, etiology, and prevention. 2020. Clin Chest Med. Mar;41(1):1-24.
Quando si parla di fattore di rischio ci si riferisce a una sostanza, abitudine o comportamento che può aumentare la probabilità di ammalarsi di tumore al polmone. Mentre alcuni fattori possono essere eliminati o ridotti, ad esempio l’abitudine al fumo, su altri non si può intervenire, come ad esempio l’avere una familiarità per la malattia o avere una determinata età. 1
È importante però comprendere che, seppure ci si esponga o ci si è esposti a uno o più fattori di rischio, non è detto che sicuramente ci si ammalerà di tumore al polmone, così come è possibile che si sviluppi la malattia in assenza di fattori di rischio. Ciò di cui si parla quando si menzionano i fattori di rischio è un’aumentata probabilità di sviluppare la malattia e non una certezza. 1
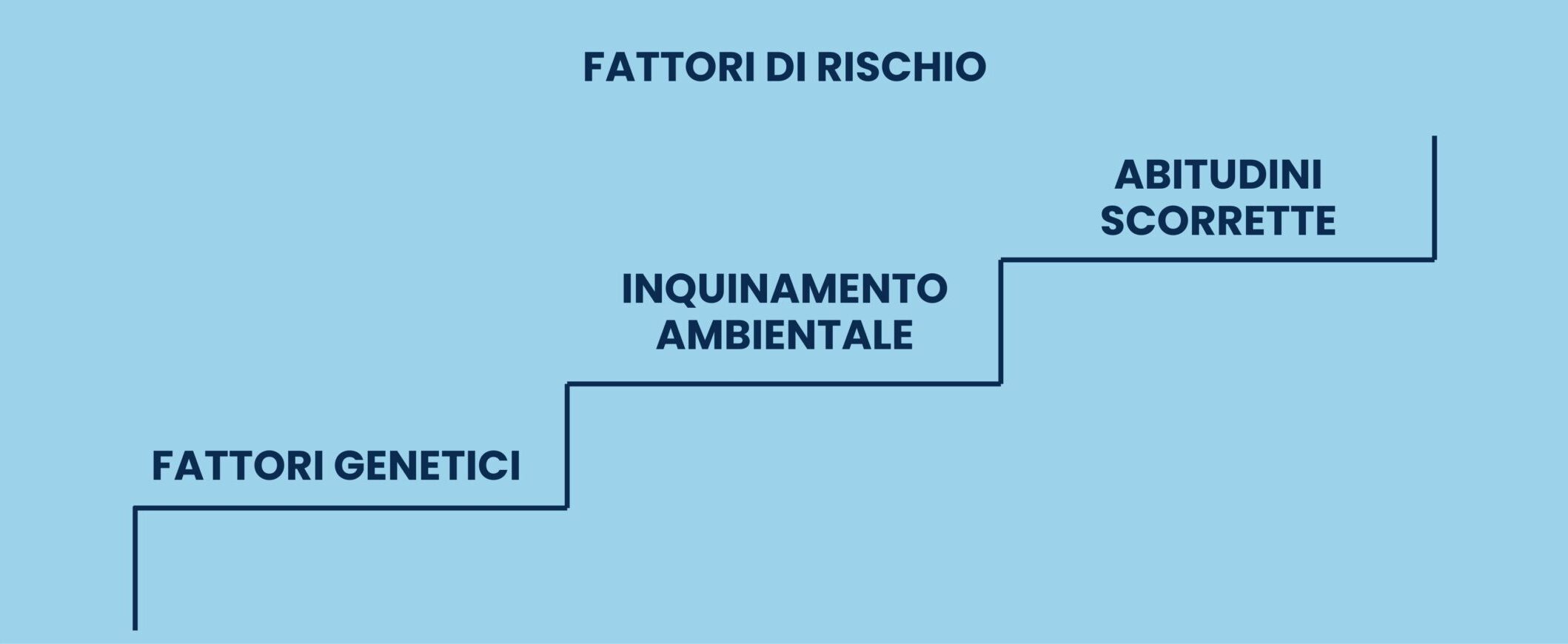
I FATTORI DI RISCHIO NEL TUMORE AI POLMONI
- Fumo: è il principale fattore di rischio per il tumore al polmone. Si stima che l’80% di tutti i pazienti che muoiono per un tumore al polmone siano fumatori e la percentuale sale quando si parla di SCLC. Quanto più si fuma e da quanto più tempo si è fumatori, tanto più le percentuali si alzano. Anche il fumo passivo rappresenta un fattore di rischio che aumenta la probabilità di ammalarsi di tumore al polmone. 1
- Amianto: le persone che sono state esposte a questo materiale, soprattutto chi ha lavorato in miniere, stabilimenti tessili o cantieri navali presentano un rischio più elevato rispetto alla popolazione generale di sviluppare tumore al polmone. Grazie alla legge n° 257 in vigore dal 1992 in Italia non è più possibile costruire con questo materiale e la maggior parte degli edifici è stata bonificata. 1
- Sostanze chimiche: composti chimici quali arsenico, silice, nickel, berillio, cadmio, cromo e derivati del carbone ma anche elementi radioattivi sono agenti definiti carcinogeni. 1
- Inquinamento: soprattutto chi vive in città molto popolate. Seppur il rischio è solo lievemente aumentato, va comunque tenuto in considerazione. 1
- Precedente storia di tumore: se ci si è già ammalati di tumore al polmone o un membro prossimo della famiglia (fratelli, sorelle, genitori) ha avuto un tumore al polmone, il rischio che si possa svilupparne uno aumenta. Va inoltre considerato che la personale esposizione a radioterapia per curare un cancro a livello del torace (polmone, seno…) è essa stessa un fattore di rischio. 1
Bibliografia
- Lung cancer risk factors. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/cancer/lung-cancer/causes-risks-prevention/risk-factors.html
Alcune tipologie di tumore al polmone presentano mutazioni di geni o proteine che possono essere utilizzati come bersaglio per specifiche terapie. 1
Se durante il processo di duplicazione delle cellule si verifica un errore, il gene si modifica creando una cosiddetta mutazione. Queste modificazioni possono essere state ereditate dai genitori (si parla quindi di mutazioni ereditarie) oppure possono verificarsi nel corso della vita (si parla di mutazioni acquisite). Alcune modifiche nei geni sono innocue mentre altre possono avere conseguenze, come ad esempio il cancro. 1
Tutti i tipi di tumore, quindi anche il tumore al polmone, insorgono a causa di mutazioni genetiche. 1

LE MUTAZIONI GENETICHE NEL TUMORE AL POLMONE
In alcune persone presentare una mutazione può renderle più suscettibili a sviluppare una certa tipologia di cancro oppure può determinare il successo o l’insuccesso di determinate terapie, così come una prognosi migliore o peggiore rispetto ad altre persone con lo stesso tumore ma che non presentano quella stessa mutazione. 2

Queste sono tra le mutazioni più comuni del tumore al polmone (dove il + dopo il nome del gene indica la presenza della mutazione). Il test mutazionale (noto anche come profilo molecolare) è un esame effettuato su cellule cancerose prelevate mediante biopsia, oppure durante l’intervento chirurgico di rimozione del tumore, che consente di conoscere se il tumore presenta specifiche mutazioni. 3
Conoscere la presenza di specifiche mutazioni del tumore al polmone è un’informazione importante, può essere d’aiuto nel decidere quale sia il trattamento migliore. 3
I tipi di cancro al polmone sono molti e possono generare non poca confusione, ma è importante conoscere la mutazione del proprio. Se si hanno dubbi e domande, non bisogna aver timore di chiedere ai medici.
Bibliografia
- Testing for gene mutations in lung cancer. Cancer Research UK. Disponibile al sito: https://www.cancerresearchuk.org/about-cancer/lung-cancer/getting-diagnosed/tests/testing-for-gene-mutations
- Precision or Personalized Medicine. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/treatment/treatments-and-side-effects/treatment-types/precision-medicine.html
- Test for lung cancer. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/cancer/lung-cancer/detection-diagnosis-staging/how-diagnosed.html
A seguito della diagnosi di tumore al polmone, vengono svolti ulteriori esami per valutare quanto il tumore si è esteso in polmoni, linfonodi e nel resto del corpo. Questo processo è chiamato stadiazione e consente di conoscere il tipo di tumore e in che stadio di sviluppo si trova e, di conseguenza, quale sia il trattamento necessario. 1
LA STADIAZIONE DEL NSCLC
I medici utilizzano il sistema TNM, in cui: 2

Tramite un sistema di numeri romani e lettere, è possibile classificare la malattia negli stadi da IA (stadio uno A=stadio iniziale) a IV (stadio quattro=tumore metastatico). 3 All”interno di ciascuno di questi stadi, la gradazione di T, N e M tramite numeri da 0 a 4 fornisce ulteriori informazioni sul tumore riguardo questi 3 parametri presi in oggetto. 2
Tra i test di laboratorio che possono essere richiesti dallo specialista, oltre al profilo genetico per la ricerca di mutazioni, c’è quello per la ricerca dell’espressione di determinate proteine nelle cellule tumorali, come PD-L1, che può dare un’indicazione sulla risposta a determinate terapie (immunoterapia). 4
Alla fine del percorso diagnostico, si arriverà ad avere un quadro chiaro del tumore: di che tipo è, quanto è esteso, se ha metastatizzato e in che stadio si trova.

Esistono 4 gradi di T che consentono di fornire indicazioni sull’estensione e posizione della massa tumorale rispetto alla sede di origine nei polmoni. 2

I gradi principali di N sono 3 e consentono di indicare il grado di coinvolgimento dei linfonodi più o meno vicini ai polmoni. 2

Esistono 2 gradi di M, che indicano se il tumore ha colonizzato altre parti del corpo al di fuori del polmone tramite metastasi oppure se è rimasto localizzato. 2
LA STADIAZIONE DEL MICROCITOMA
Il microcitoma presenta soltanto due possibili stadi basati sul grado di estensione del tumore: malattia limitata oppure malattia estesa. 2
Bibliografia
1.How Is Lung Cancer Diagnosed and Treated? Center for Disease Control and Prevention (CDC). Disponibile al sito: https://www.cdc.gov/cancer/lung/basic_info/diagnosis_treatment.htm
2.Lung cancer. Diagnosis. National Health Service (NHS). Disponibile al sito: https://www.nhs.uk/conditions/lung-cancer/diagnosis/
3.Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
A volte scoprire di avere il tumore al polmone può avvenire per pura causalità se non si presentano sintomi caratteristici, ad esempio durante una radiografia richiesta per altri motivi. 1
Gli esami richiesti per la diagnosi del tumore al polmone comprendono le analisi del sangue 2 e la radiografia al torace che possono aiutare a escludere altre cause dei sintomi, come ad esempio un’infezione 3 , oltre a ulteriori esami strumentali. 2
GLI ESAMI STRUMENTALI NELLA DIAGNOSI DI TUMORE AL POLMONE
- La radiografia al torace: di solito è il primo esame strumentale che viene prescritto sebbene non fornisca una diagnosi definitiva di tumore al polmone, poiché non riesce a distinguere la natura delle “macchie” osservate. 2
- Per questo motivo, successivamente alla radiografia, viene prescritta una TC (tomografia computerizzata) con mezzo di contrasto che consente di ottenere immagini dettagliate dell’interno del corpo. 2
- Se la TC mostra la presenza di tumore al polmone in stadio precoce, è possibile che venga prescritta una PET-TC (tomografia a emissione di positroni) per localizzare le cellule tumorali attive. 2
- La broncoscopia viene prevista nel caso in cui la TC abbia evidenziato la massa tumorale al centro del petto; si tratta di una procedura che consente di vedere l’interno delle vie aeree grazie a un sottile tubicino dotato di una telecamera e di prelevare un piccolo campione di cellule tumorali, chiamato biopsia. Oggi è inoltre possibile ricorrere a una procedura di broncoscopia innovativa chiamata EBUS che ricorre a una sonda a ultrasuoni per localizzare anche i linfonodi da cui prelevare una biopsia per la loro valutazione. 2
- La biopsia consente di definire la tipologia stessa del tumore 2 e di poter eseguire i test genetici per identificare quali geni mutati sono responsabili del tumore, consentendo così di avere ulteriori informazioni prima di iniziare la terapia. 2
Tra i test di laboratorio che possono essere richiesti dallo specialista, oltre al profilo genetico per la ricerca di mutazioni, c’è quello per la ricerca dell’espressione di determinate proteine nelle cellule tumorali, come PD-L1, che può dare un’indicazione sulla risposta a determinate terapie (immunoterapia). 4
Alla fine del percorso diagnostico, si arriverà ad avere un quadro chiaro del tumore: di che tipo è, quanto è esteso, se ha metastatizzato e in che stadio si trova.
Bibliografia
1.Lung cancer symptoms. Cancer Research UK. Disponibile al sito: https://www.cancerresearchuk.org/about-cancer/lung-cancer/symptoms
2.Lung cancer. Diagnosis. National Health Service (NHS). Disponibile al sito: https://www.nhs.uk/conditions/lung-cancer/diagnosis/
3.What to know about pneumonia and lung cancer. Medical News Today. Disponibile al sito: https://www.medicalnewstoday.com/articles/316783#risk-factors .
4.Test for lung cancer. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/cancer/lung-cancer/detection-diagnosis-staging/how-diagnosed.html
5.Testing for gene mutations in lung cancer. Cancer Research UK. Disponibile al sito: https://www.cancerresearchuk.org/about-cancer/lung-cancer/getting-diagnosed/tests/testing-for-gene-mutations
Per screening si intende l’esecuzione di test diagnostici in tutti i componenti di una popolazione sana ma considerata a rischio con l’obiettivo di effettuare una diagnosi precoce.
I criteri che una persona deve soddisfare per essere considerata “a rischio” sono due:
- Età tra i 50 e i 75 anni.1
- Essere fumatori di almeno 20-30 pacchetti di sigaretta/anno oppure essere ex fumatori che hanno smesso di fumare da meno di 10 anni.1
I centri più importanti per lo screening sono:
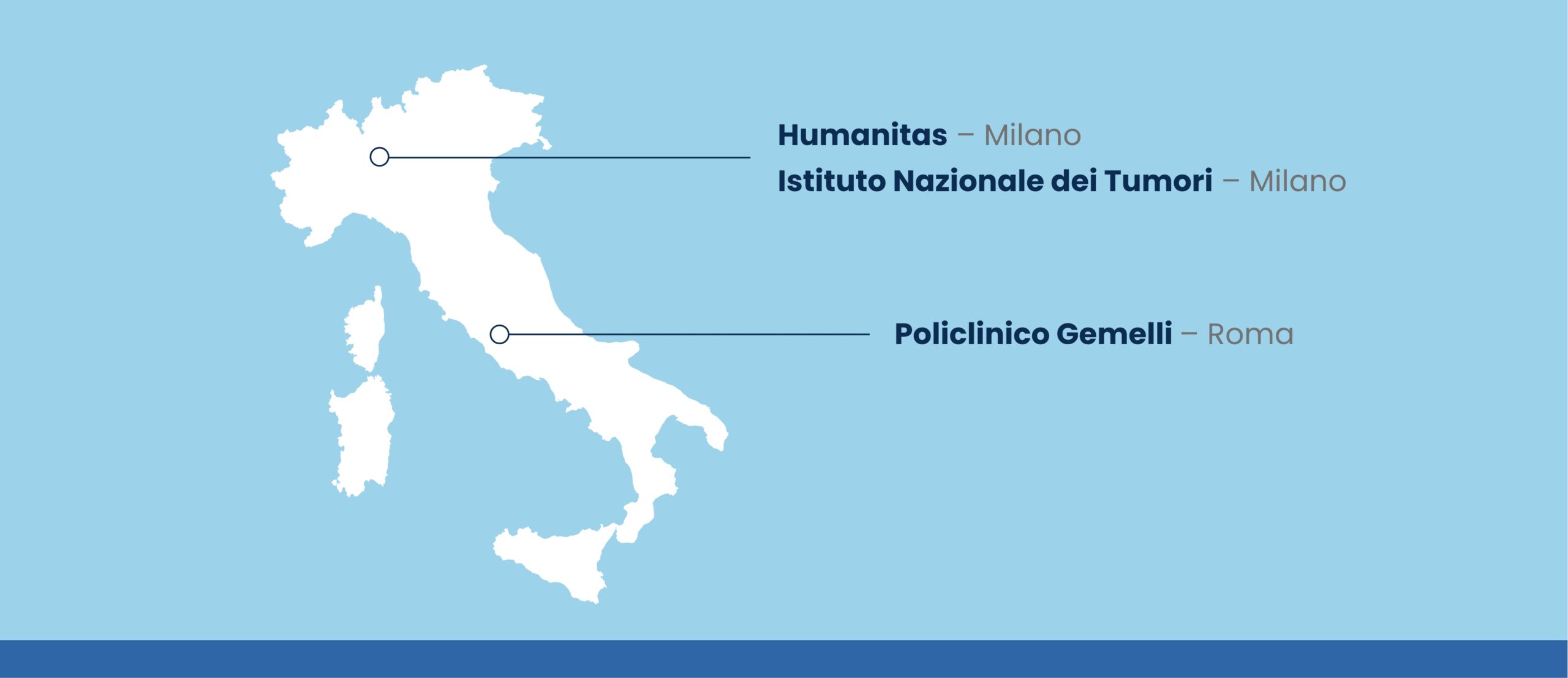
Ma, in generale, in tutta Italia esistono strutture che forniscono gratuitamente lo screening, spesso all’interno di programmi di studio e di ricerca.

Il National Lung Screening Trial (NLST) è stato il primo studio a dimostrare come la diagnosi precoce di tumore polmonare con TC al torace a bassa dose, annuale, in soggetti ad alto rischio, determini una riduzione della mortalità associata a tale malattia del 20%. 3 In Europa sono stati completati, e sono tutt’ora in corso, molti studi dedicati allo screening del tumore polmonare. 4 In particolare lo studio italiano MILD ha recentemente dimostrato che l’esecuzione della TC al torace a bassa dose in soggetti fumatori ad alto rischio per tumore polmonare: 4
- con frequenza annuale o biennale
- per un periodo totale di 10 anni
- si associa a una riduzione della mortalità a 10 anni pari al 39% rispetto alla sola osservazione 4
Anche lo studio belga NELSON, condotto su 12.195 uomini e 2594 donne, conferma che l’utilizzo della TC a bassa dose riduce significativamente la mortalità causata dal tumore al polmone. 5
Bibliografia
- Oudkerk M, et al. European position statement on lung cancer screening. Lancet Oncol. 2017;18(12):e754-e766; 2. Markowitz SB, et al. Capacità della TC spirale a bassa dose di radiazione di distinguere tra noduli polmonari non calcifici benigni e maligni. Chest. Edizione italiana. IX. 2007; 3. National Lung Screening Trial Research Team, Aberle DR, Adams AM, Berg CD, et al. Reduced lung-cancer mortality with low-dose computed tomographic screening. N Engl J Med. 2011;365:395-409; 4. Linee Guida AIOM. Tumore al polmone. 2019; 5. de Koning HJ, et al. Reduced lung-cancer mortality with volume CT-screening in a randomized trial. N Engl J Med. 2020 Feb 6;382(6):503-513.
Molto di rado il microcitoma, e solamente se in stadio limitato, può essere operato.1 In genere, il trattamento di scelta è la terapia sistemica, cioè una terapia medica che permette un controllo generalizzato della malattia.1

CHEMIOTERAPIA
La terapia sistemica classica è la chemioterapia, somministrata da sola o in associazione alla radioterapia. 2 Con la chemioterapia si somministrano farmaci specifici, detti citotossici, che vanno a bloccare la crescita e distruggere le cellule tumorali presenti, cercando così non solo di rallentare la crescita del tumore, ma anche di ridurne le dimensioni.3
Esistono due tipi di chemioterapia: quella in cui si somministra un solo farmaco, chiamata monochemioterapia, e quella in cui si somministrano due o più farmaci, detta polichemioterapia. 1
Nel microcitoma si usa la polichemioterapia perché più efficace nel contrastarlo. 1
IMMUNOTERAPIA
Accanto alla chemioterapia, per il trattamento del microcitoma recentemente si è resa disponibile l’immunoterapia, somministrata in associazione, e successivamente, alla chemioterapia.4
Il principio dell’immunoterapia è molto differente da quello della chemioterapia: il farmaco immunoterapico agisce sul sistema immunitario e lo stimola a colpire e distruggere solo le cellule tumorali; nel secondo caso invece, il farmaco chemioterapico agisce su tutte le cellule che replicano velocemente, come le cellule tumorali, ma anche altre cellule utili all’organismo, quali i globuli rossi, le piastrine e i follicoli piliferi.5
Il risultato di questo diverso meccanismo d’azione si osserva soprattutto in termini di tossicità: la chemioterapia provoca effetti collaterali marcati, tra cui la perdita dei capelli, mentre l’immunoterapia ha effetti collaterali diversi, ma solitamente più gestibili, quali stanchezza, pruriti, irritazioni cutanee ma anche coliti e diarrea, febbre, dolori a ossa e articolazioni.5
RADIOTERAPIA
La radioterapia consiste in radiazioni ionizzanti che hanno lo scopo di distruggere le cellule tumorali senza danneggiare i tessuti sani circostanti. 6
Il bersaglio delle radiazioni è il DNA delle cellule tumorali che, una volta danneggiato, provoca la morte della cellula, portando alla diminuzione delle dimensioni del tumore. 6
Nel caso del microcitoma, la radioterapia si effettua sul torace, la zona del corpo in cui origina il tumore, ma in alcuni casi può essere svolto un trattamento di radioterapia anche al di fuori del torace, per trattare specifiche metastasi a distanza (ad esempio, al cervello), alleviarne i sintomi (radioterapia a scopo palliativo) o infine prevenire la comparsa di metastasi cerebrali. 1
MALATTIA LIMITATA
Con “malattia limitata” si indica una situazione in cui il microcitoma è presente solo in una metà del torace, senza metastasi in altri organi. 1
In casi molto rari la malattia può essere operata, ma nella grandissima parte dei casi la terapia di scelta più efficace è una combinazione di chemioterapia e radioterapia, con una polichemioterapia che vede l’impiego di farmaci quali platino ed etoposide, contemporaneamente. 1
Questo trattamento può provocare diversi effetti collaterali quali: anemia, maggiore suscettibilità alle infezioni, caduta di capelli, nausea e vomito, a causa della combinazione di farmaci/radiazioni, ma il suo impiego è giustificato dall’elevata efficacia terapeutica e dalla diminuzione della possibilità che la malattia si ripresenti. 1
L’oncologo potrebbe anche valutare la possibilità di effettuare una radioterapia profilattica sull’encefalo (PCI) con l’obiettivo di prevenire la formazione di eventuali metastasi a livello cerebrale. 1
Nel quadro clinico della malattia limitata non ci sono attualmente dati che supportino l’impiego dell’immunoterapia.7
MALATTIA ESTESA
Con “malattia estesa” si intende una situazione in cui, alla malattia presente a livello del torace, si aggiungono una o più metastasi a distanza. 1
La radioterapia è solitamente sconsigliata in questi casi, in quanto l’area da trattare (il torace e le aree in cui si sono localizzate le metastasi) sarebbe troppo estesa e la terapia perderebbe di efficacia. 1
Questa condizione prevede, invece, l’intervento della sola chemioterapia a base di platino ed etoposide, a cui è ora possibile associare l’immunoterapia.1 Quest’ultima è considerata ad oggi la terapia di scelta in prima linea nel trattamento di microcitoma in stadio esteso ed è somministrata sia durante la chemioterapia che per un periodo successivo alla conclusione dei cicli di chemio.7
Anche in questo caso può essere consigliata la PCI se si è avuta una buona risposta alla chemioterapia. 1
BIBLIOGRAFIA
- Sito web AIOT – AIOTOWN, 5. Percorso terapeutico – F. Terapia del microcitoma o carcinoma polmonare a piccole cellule (SCLC)
- Microcitoma polmonare, dalla diagnosi alla cura. Una guida per i pazienti. WALCE. A cura di S. Novello et al.
- Sito web AIOT – AIOTOWN, 5. Percorso terapeutico – C. Chemioterapia ed effetti collaterali
- Tay RY, et al. Lung Cancer. 2019; 137:31-37
- Sito web AIOT – AIOTOWN, 5. Percorso terapeutico – G. Immunoterapia
- Sito web AIOT – AIOTOWN, 5. Percorso terapeutico – B. Radioterapia ed effetti collaterali
- Linee guida NCCN – Small cell lung cancer V.1.2023 – Aug. 25, 2022
Il carcinoma polmonare a piccole cellule (SCLC – Small Cell Lung Cancer) o microcitoma è così definito perché al microscopio le cellule tumorali appaiono di piccole dimensioni con una tipica forma di chicchi d’avena. 1
Il microcitoma rappresenta il 10-15% di tutti i tumori polmonari. 1 È considerato un tumore aggressivo a causa della velocità con cui aumenta di dimensioni e per l’elevata capacità di metastatizzare a distanza e in tempi brevi ed è caratterizzato dall’elevato tasso di recidive, ossia di episodi in cui la malattia ricompare dopo l’iniziale risposta alla terapia. 2
Il microcitoma è definito un tumore neuroendocrino perché origina dalle cellule del polmone definite, appunto, neuroendocrine che hanno cioè caratteristiche sia delle cellule che rilasciano ormoni (endocrine) sia delle cellule nervose. 2
La quasi totalità dei casi di microcitoma origina nel polmone e solo una piccolissima percentuale origina in sedi diverse quali la nasofaringe, il tratto gastrointestinale e il genitourinario. 2

BIBLIOGRAFIA
- About lung cancer. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/content/dam/CRC/PDF/Public/8703.00.pdf
- Small Cell Lung Cancer: Clinical Practice Guidelines in Oncology. NIH-PA. J Natl Compr Canc Netw. 2013;11:78–98.
La sorveglianza è il processo attraverso il quale il sistema immunitario riconosce i tumori e dà inizio a una risposta anti-tumorale. 1

Sulla superficie delle cellule tumorali sono presenti alcune strutture differenti rispetto a quelle presenti sulle cellule sane: sono i cosiddetti antigeni tumorali, che permettono al sistema immunitario di riconoscere la cellula malata come estranea. 1
- Specifiche cellule del sistema immunitario definite cellule che presentano l’antigene (APC) sono deputate al riconoscimento di questi antigeni estranei. Nel momento in cui le APC individuano una cellula tumorale possono attivare a loro volta i linfociti, i quali sono in grado di attaccare il tumore. 1
- In alcuni casi però le cellule tumorali evadono il controllo del sistema immunitario, generando un ambiente che non promuove la risposta anti-tumorale, definito immunosoppressivo. 2
- Ciò provoca la replicazione delle cellule tumorali in modo incontrollato, determinando così lo sviluppo e la crescita del tumore. 1
Bibliografia
- Boldrini M, Smerrieri S, Cabra P. Immuno-oncologia. 100 domande 100 risposte. La guida per conoscere la nuova arma contro i tumori e il “pianeta” cancro. Seconda edizione. AIOM
- Beatty GL, et al. Immune escape mechanisms as a guide for cancer immunotherapy. Clin Cancer Res. 2015;21(4):687-92
A oggi sono state identificate oltre 12 mutazioni genetiche correlate al NSCLC, alcune delle quali sono più comuni di altre. 1
Tali mutazioni possono insorgere in tutte le diverse forme di NSCLC, ma è stato osservato che sono più frequenti in alcuni specifici gruppi di pazienti. 1
Conoscere la presenza di queste mutazioni è fondamentale per poter scegliere il trattamento più adeguato ed efficace. 1
INCIDENZA DI MUTAZIONI SPECIFICHE NELL’NSCLC 1
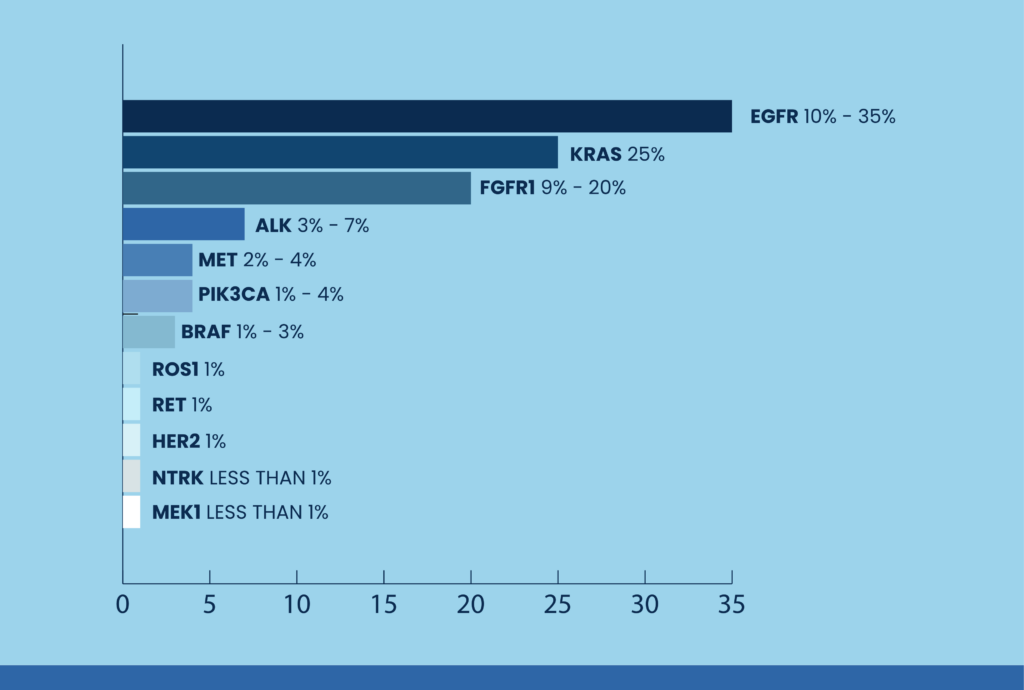
EGFR
Il gene controlla una proteina chiamata recettore per il fattore di crescita epidermico (EGFR) coinvolta nella regolazione della crescita e proliferazione della cellula. È più comune nei pazienti donne, non fumatori, con adenocarcinoma. 1
ALK
È il gene che codifica per la chinasi del linfoma anaplastico; quando è presente tale mutazione due geni si fondono insieme per crearne uno nuovo. Tale mutazione è presente in persone che non hanno mai fumato o hanno ceduto raramente al fumo. È una mutazione molto comune in persone cinquantenni e negli uomini. 1
HER2
Quando questo gene è mutato le cellule tumorali sono spinte a crescere. Questa mutazione si riscontra soprattutto nelle donne e in persone che non hanno mai fumato o hanno fumato raramente. 1
ROS1
Questa mutazione è simile a quella ALK per quanto riguarda le popolazioni colpite: cinquantenni e non fumatori. 1
KRAS
Questo gene permette che venga prodotta una proteina chiamata K-Ras che aiuta le cellule a crescere e a dividersi. 1
NTRK
In coloro che hanno questa mutazione il gene NTRK si fonde con altri geni e non ci sono caratteristiche specifiche negli individui in cui viene trovata: sia fumatori che non e di ogni fascia d’età. 1
RET
Letteralmente è il «gene riarrangiato durante la trasfezione» ed è particolarmente comune nei soggetti non fumatori. 1
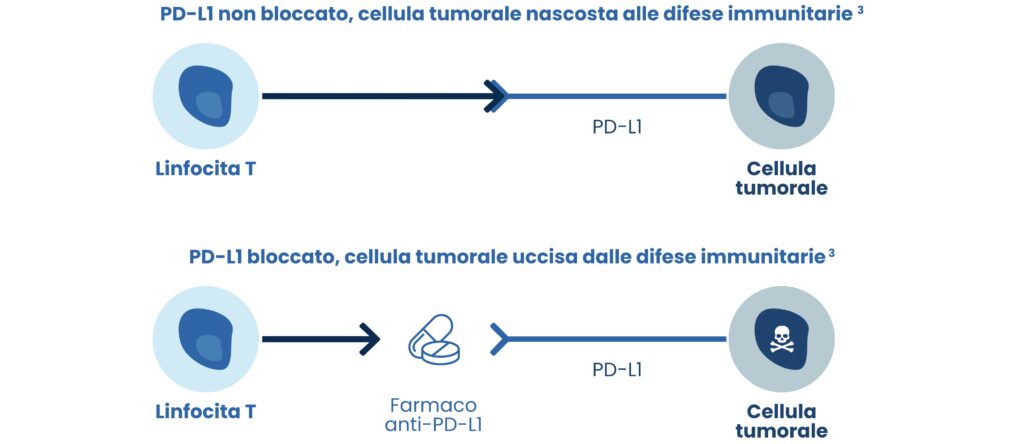
PD-L1
Il ligando di morte programmata 1, o PD-L1, è una proteina coinvolta nei meccanismi che il tumore mette in atto per sfuggire alle difese immunitarie del corpo. 2 Per decidere come trattare al meglio un tumore e a quali terapie è possibile sottoporre il paziente è importante valutare in che misura questa proteina è presente nel tumore. 3
IL RUOLO DI PD-L1
Sulla superficie dei linfociti T, un particolare tipo di globuli bianchi è presente un recettore che, tramite il legame alla proteina PD-L1, riconosce se una cellula appartiene o meno al nostro organismo. 3 Il tumore, grazie alla presenza sulla superficie delle sue cellule di PD-L1, è in grado di legarsi ai linfociti e “mascherandosi” da una cellula dell’organismo, nascondendosi di fatto alle difese immunitarie. I linfociti perciò sono indotti a non riconoscere la cellula come tumorale e non danno avvio al processo di eliminazione delle cellule tumorali. 3 Per far sì che il sistema immunitario torni a riconoscere le cellule tumorali come non appartenenti al corpo si sono sviluppati dei nuovi farmaci detti anti-PD-L1. 3 Tali farmaci si legano a PD-L1 sulle cellule tumorali impedendogli di legarsi quindi ai linfociti che in questo modo possono riconoscere la cellula tumorale come estranea al corpo e attivare la risposta immunitaria. 3
I TEST PER LE MUTAZIONI GENETICHE
Per effettuare i test utili a identificare la presenza di eventuali mutazioni è necessario raccogliere un campione del tumore. Questo avviene con una delle seguenti modalità: 1
- Tramite broncoscopia, ossia prelevando un campione di tumore dal polmone, tramite un piccolo tubicino che si fa passare dalla bocca o dal naso (nessuna paura, si è anestetizzati per la procedura).
- Usando un sottilissimo ago che il medico inserisce direttamente dal petto (si può prelevare anche del liquido dai polmoni). Questa procedura è chiamata agobiopsia transtoracica.
- Una variante di quest’ultima procedura è la VATS, cioè la toracoscopia chirurgica video-assistita. Il medico, invece di inserire un ago nel petto, fa un piccolo taglietto e inserisce un tubicino con cui preleva il tessuto.
- A differenza della VATS, se il taglio viene effettuato in un punto specifico sopra lo sterno, parliamo di mediastinoscopia ma la procedura è simile.

Una volta ottenuto il campione di tessuto tumorale, l’analisi delle mutazioni può essere condotta con le seguenti modalità:
- Immunoistochimica: consente di evidenziare l’espressione di determinate proteine, definite marker tumorali. Serve il tessuto tumorale per fare questo tipo di test. 1
- FISH: è un acronimo che indica un test di fluorescenza che ricerca specifiche variazioni nei geni. Per questo tipo di test può essere usato sia il sangue sia il tessuto proveniente dal tumore. 1
- Test allele-specifico: è un test che permette di analizzare il DNA per una singola, specifica mutazione. 1
- NGS: si tratta di un acronimo che indica ”sequenziamento genetico di nuova generazione” e permette di individuare mutazioni diverse, effettuando però il test una sola volta. È più veloce di altri test e si può effettuare sia su sangue sia su tessuto tumorale. 1
Bibliografia
- Gene mutations in Non-Small-Cell Lung Cancer. Disponibile al sito: https://www.webmd.com/lung-cancer/story/nsclc-gene-mutations
- Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
- Caldwell C. et al. Sci Rep. 2017;7:13682
- Cancer Research UK. FISH testing. Disponibile al sito: https://www.cancerresearchuk.org/about-cancer/cancer-in-general/tests/fish
DNA
Lo studio delle caratteristiche molecolari dei tumori al polmone ha evidenziato un ruolo specifico per alcuni geni, tra cui un gene denominato EGFR. 1
I geni rappresentano importanti bersagli per alcuni farmaci.
La determinazione di mutazioni di EGFR si rende necessaria per la scelta della migliore strategia terapeutica. 1
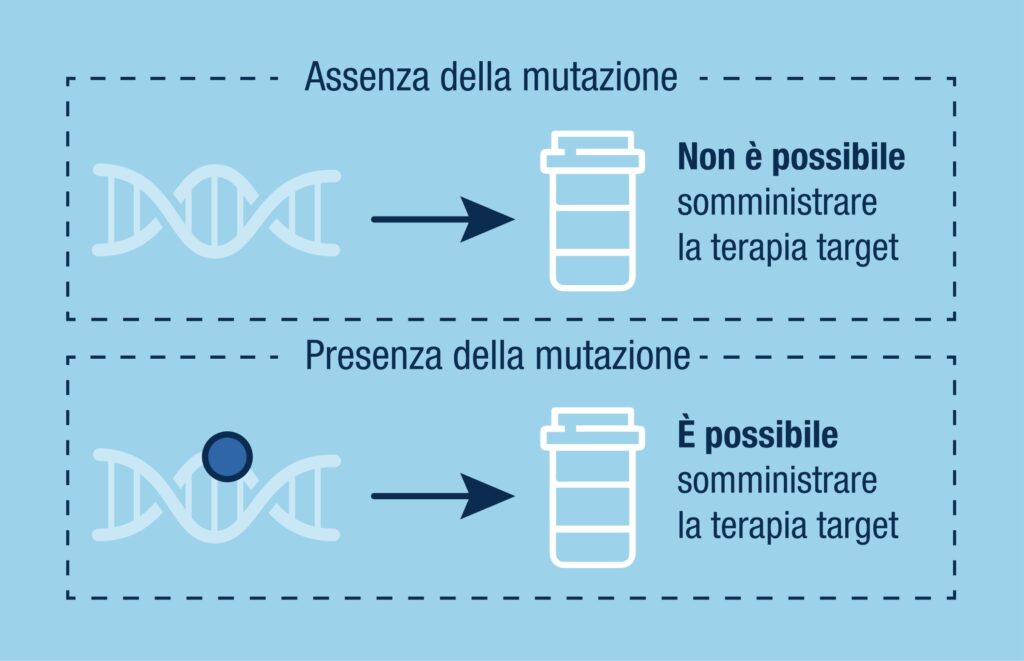
PROTEINE
Nel tumore al polmone è importante inoltre valutare un altro marcatore noto come PD-L1.1
PD-L1 è una proteina presente sulla membrana delle cellule tumorali.2
Valutare la quantità della proteina PD-L1 permette di prevedere l’efficacia dell’immunoterapia.2
COS’È UN MARCATORE BIOLOGICO?
Un marcatore biologico o biomarcatore è un indicatore che può essere misurato in modo affidabile e che ci può dare informazioni riguardo lo stato di malattia dell’individuo.
I biomarcatori possono essere:
- Variazioni nella sequenza del DNA
- Sostanze biologiche di origine proteica, rilevabili nel sangue o in campioni di tessuto
L’identikit molecolare del tumore al polmone si effettua valutando alcuni biomarcatori, utili per predire se un paziente risponderà o meno a una specifica terapia. 1
- La valutazione delle mutazioni del gene EGFR è utile per valutare la prescrizione di una terapia specifica, definita a bersaglio molecolare. 1
- La valutazione del livello della proteina PD-L1 è uno dei parametri che viene preso in considerazione per la scelta del trattamento nei pazienti con NSCLC; in particolare per poter somministrare l’immunoterapia. 1
Bibliografia
- Linee Guida AIOM. Tumore al polmone. 2019
- IASCL atlas testing od PD-L1 immunoistochemistry testing in lung cancer. Edited by MS Tsao, et al. 2017
Il NSCLC origina dalle cellule epiteliali dei polmoni, dai bronchi centrali agli alveoli terminali. 1
Le tre principali forme di NSCLC sono l’adenocarcinoma, il carcinoma a cellule squamose e il carcinoma a grandi cellule. 2
Esistono tuttavia numerose altre tipi di NSCLC, che sono meno frequenti. 1

ADENOCARCINOMA
Costituisce la forma di NSCLC più comune 1 e rappresenta il 40% di tutti i tumori polmonari maligni. 4 Ha origine dalle cellule secernenti muco che rivestono la superficie interna delle vie respiratorie, 3 solitamente nel tessuto polmonare periferico. 1
Si verifica prevalentemente tra i fumatori, nelle donne e rappresenta il tumore polmonare più frequente nella popolazione giovane. 2
CARCINOMA A CELLULE SQUAMOSE
Costituisce il 25-30% di tutti i tumori polmonari, 4 ha origine a livello delle cellule che rivestono le vie respiratorie e tende a crescere al centro del polmone. 3 È più frequente tra i fumatori. 2
CARCINOMA A GRANDI CELLULE
Rappresenta il 10-15% di tutti i tumori polmonari e prende il nome dall’aspetto al microscopio delle cellule che lo compongono. 4
Può insorgere in qualsiasi area del polmone e tende a crescere rapidamente. 2
Bibliografia
- General Information About Non-Small Cell Lung Cancer (NSCLC). National Cancer Institute (NIH). Disponibile al sito: https://www.cancer.gov/types/lung/hp/non-small-cell-lung-treatment-pdq
- What is lung cancer. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/cancer/lung-cancer/about/what-is.html
- Types of lung cancer. Cancer Research UK. Disponibile al sito: https://www.cancerresearchuk.org/about-cancer/lung-cancer/stages-types-grades/types
- Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
I sintomi del tumore ai polmoni sono diversi e non sempre sono specifici. Alcune persone, infatti, sviluppano sintomi legati ai polmoni, altre manifestano sintomi legati alla parte del corpo in cui il tumore si è esteso (metastatizzato) e altri ancora possono manifestare sintomi generici. 1 Nella maggior parte dei casi, tuttavia, il tumore al polmone non provoca alcun sintomo nelle fasi iniziali della malattia. 2
Trattandosi di sintomi perlopiù comuni anche ad altre malattie, non è sempre facile attribuirli al tumore al polmone e capita che la diagnosi della malattia avvenga per caso nel corso di analisi radiologiche effettuate per altre patologie. 3
A seguito dell’insorgenza dei primi sintomi è fondamentale rivolgersi al medico di fiducia che, dopo valutazione, prescriverà gli esami necessari ad accertare la natura degli stessi, inviando allo specialista.

I SINTOMI DEL TUMORE AI POLMONI
I sintomi più comuni del tumore al polmone possono includere: 2
- Tosse persistente o che peggiora nel tempo; è uno dei sintomi più frequenti, può essere sia tosse secca sia tosse con catarro oppure un peggioramento della solita “tosse del fumatore”.3
- Presenza di sangue quando si tossisce o espettorato color ruggine (saliva o catarro).
- Dolore al petto che spesso peggiora se respirando profondamente, tossendo o ridendo.
- Raucedine.
- Perdita dell’appetito.
- Perdita di peso inspiegabile.
- Affanno (dispnea).
- Sensazione di stanchezza o debolezza.
- Infezioni persistenti o ricorrenti, come bronchite o polmonite.
- Comparsa di rumore sibilante con la respirazione.
Se il tumore al polmone si estende anche in altre parti del corpo, può provocare: 2
- Dolore osseo (ad esempio mal di schiena o dolore alle anche).
- Manifestazioni a carico del sistema nervoso causate dalla diffusione del cancro fino al cervello (ad esempio mal di testa, debolezza o intorpidimento di un braccio o una gamba, capogiri, problemi di equilibrio o convulsioni).
- Ingiallimento della pelle e degli occhi (ittero) dato dalla diffusione del tumore nel fegato.
- Ingrossamento dei linfonodi (ad esempio di collo o sopra le clavicole).
Bibliografia
1.What are the symptoms of lung cancer? Center for Disease Control and Prevention (CDC). Disponibile al sito: https://www.cdc.gov/cancer/lung/basic_info/symptoms.htm .
2.Signs and symptoms of lung cancer. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/cancer/lung-cancer/detection-diagnosis-staging/signs-symptoms.html .
3.Sintomatologia del tumore polmonare. AIOTown. Disponibile al sito: https://www.oncologiatoracica.it/public/town/D%20Sintomatologia.pdf .
Esistono due principali tipi di tumore al polmone, classificati secondo la tipologia di cellule nelle quali il tumore inizia a svilupparsi: 1
- carcinoma polmonare non a piccole cellule (NSCLC).
- carcinoma polmonare a piccole cellule (SCLC).
La tipologia di tumore al polmone determina la terapia. 1
Il tumore che ha origine dai polmoni è chiamato “primitivo” mentre, se si diffonde ai polmoni da tumori presenti in altre parti del corpo, prende il nome di tumore “secondario”. 1

Carcinoma polmonare non a piccole cellule (non-small cell lung cancer, NSCLC)
Il NSCLC costituisce l’80-85% delle forme di tumore al polmone. I tre principali sottotipi del NSCLC sono: 2
- adenocarcinoma
- carcinoma a cellule squamose
- carcinoma a grandi cellule
Il microcitoma o carcinoma polmonare a piccole cellule (small-cell lung cancer, SCLC)
Il microcitoma costituisce il 10-15% delle forme di tumore al polmone. Questa tipologia di tumore al polmone tende ad avere una crescita e un’espansione più rapide del NSCLC. In circa 70% delle persone con SCLC al momento della diagnosi il tumore è già esteso. Data la sua rapida crescita, tende a rispondere bene ad alcune terapie, tuttavia nella maggior parte dei casi si ripresenterà. 2
Bibliografia
1.Lung cancer – Overview. National Health Service (NHS). Disponibile al sito: https://www.nhs.uk/conditions/lung-cancer/.
2.What is lung cancer?. American Cancer Society (ACS). Disponibile al sito: https://www.cancer.gov/types/lung/hp/non-small-cell–lung-treatment.
Come in molti altri ambiti, non esiste un unico trattamento per il tumore al polmone; questo dipende infatti dallo stadio, dalla mutazione che il cancro al polmone presenta e anche dal paziente. È giusto infatti che a ogni paziente sia chiesta un’opinione su quale trattamento preferisce. 1
In alcuni casi, inoltre, il medico decide di procedere con più di un trattamento, combinandoli per renderli più efficaci. 1
PRINCIPALI TRATTAMENTI A DISPOSIZIONE PER IL TUMORE AL POLMONE IN FASE INIZIALE1
Intervento chirurgico: indicato per l’NSCLC in stadio iniziale. Ci sono 3 modalità diverse con cui si interviene:
- rimuovendo una parte molto piccola del polmone, l’intervento viene chiamato resezione segmentaria;
- rimuovendo una parte maggiore e delimitata del polmone (detta lobo), da qui il nome lobectomia;
- rimuovendo l’intero polmone, in questo caso si parla di pneumonectomia.
Chemioterapia: si tratta il tumore con farmaci che uccidono le cellule tumorali. La chemioterapia può essere fatta prima dell’intervento chirurgico, per diminuire le dimensioni del tumore, o subito dopo1 per eradicare l’eventuale presenza ancora di malattia o prevenire eventuali successive ricadute.2
Radioterapia: grazie a radiazioni ad elevata energia (ionizzanti) si danneggiano le cellule tumorali così da causarne la morte. Può essere utilizzata per trattare il tumore al polmone sia in stadio precoce, sia in stadio più avanzato.1
Chemioradioterapia: è un trattamento combinato che consiste nel ricevere contemporaneamente chemio e radioterapia.1
Ci sono poi trattamenti più innovativi e probabilmente meno universalmente noti, che però stanno dando ottimi risultati:1
- Le cosiddette terapie a bersaglio molecolare: hanno lo stesso scopo della chemioterapia, cioè eliminare le cellule tumorali, ma lo fanno in maniera specifica, legandosi cioè direttamente a una parte della cellula tumorale, così da non colpire le cellule sane circostanti, cosa che invece succede con la chemioterapia.
- Le terapie anti-angiogeniche: il loro scopo è impedire al tumore di formare nuovi vasi sanguigni, che gli servono per crescere di dimensione e per espandersi.
- L’immunoterapia: i tumori sono in grado di «nascondersi» al sistema immunitario tramite diversi meccanismi. L’immunoterapia blocca questi meccanismi così che il sistema immunitario possa attivarsi per combattere il tumore.
BIBLIOGRAFIA
- Cancro del polmone non a piccole cellule (NSCLC). Guida ESMO per il paziente. Disponibile al sito: https://www.esmo.org/content/download/87433/1608958/1/IT-Cancro-del-Polmone-non-a-Piccole-Cellule-NSCLC-Guida-per-il-Paziente.pdf
- How Is Chemotherapy Used to Treat Cancer? American Cancer Society (ACS). Disponibile al sito: https://www.cancer.org/treatment/treatments-and-side-effects/treatment-types/chemotherapy/how-is-chemotherapy-used-to-treat-cancer.html
